
Микроэлементы
Интересно, какие из более чем девяноста встречающихся в природе элементов являются, собственно, жизненно необходимыми? "Строительный материал" всего живого (аминокислоты, нуклеотиды, сахара) состоит из углерода, азота, водорода, фосфора и серы. Для поддержания электролитного баланса в клетках и жидкостях организма требуются большие количества ионов натрия, кальция, калия, магния и хлора, а также фосфора и серы (в виде фосфатов и сульфатов). Для чего же нужны очень небольшие количества микроэлементов, доля которых составляет менее 0,01% массы тела?
Большинство микроэлементов незаменимо для функционирования многих жизненно важных ферментов, их коферментов или простетических групп. Поскольку они используются в ферментах миллионы раз, потребности организма в микроэлементах, как и в витаминах, крайне незначительны. Однако без них обмен веществ невозможен.
В химической промышленности в качестве катализатора используются главным образом металлы. Точно так же и ферменты "используют" металлы как вспомогательное средство для биологического катализа. В некоторых ферментах, так называемых металлоферментах, металлы (например, железо, медь, цинк и молибден) в неизмененном виде, в виде ионов или компонентов простетических групп прочно связаны в активном центре. При удалении этих металлов металлоферменты теряют свою функциональную активность. В активном центре металлы помогают связывать субстрат, переносить электроны и обеспечивать оптимальную пространственную конфигурацию фермента для эффективного катализа.
На примере гемогруппы мы выяснили важную роль железа. Железо участвует главным образом в реакциях переноса электронов, катализируемых оксидоредуктазами.
По крайней мере 90 ферментов содержат цинк. Цинксодержащие ферменты контролируют, например, образование CO2 и процесс переваривания белков. Цинк влияет на работу алкогольдегидрогеназы печени и ферментов, участвующих в передаче генетической информации.
Медь входит в основном в состав более десяти гидроксилаз. Медьсодержащий фермент тирозиназа катализирует, например, образование темного пигмента кожи и волос, меланина. Отсутствие или блокирование тирозиназы приводит к альбинизму. Наверняка каждый наблюдал действие растительной тирозиназы: побурение поверхности свежих срезов у яблок, картофеля и бананов. При этом ферментативным путем образуются темные, меланиноподобные пигменты. Другой медьсодержащий фермент - аскорбатоксидаза - ответствен за быстрое расщепление витамина С при производстве сушеных продуктов из картофеля, яблок и овощей.
Биологическая роль кобальта состоит прежде всего в том, что он входит в состав витамина В12 и образующихся из него коферментов. Например, в Австралии, где почвы бедны кобальтом, на начальных этапах освоения этого континента европейцами разведение овец и крупного рогатого скота происходило не совсем гладко. Из-за малого содержания кобальта в почвах животные недополучали его с кормом, и поэтому синтез витамина В12 бактериями в желудках жвачных был понижен. В результате возникали авитаминозы (В12) животных. Кобальт, кроме того, участвует в ферментативных процессах синтеза наследственного материала клетки и аминокислотного обмена.
Для образования органических соединений азота у растений необходим прежде всего азот. Почти все растения получают его за счет поглощения нитратов (NO3-) из почвы. С помощью молибденсодержащего фермента нитратредуктазы нитраты восстанавливаются с образованием усвояемой формы-аммиака. В корневых клубеньках бобовых растений (например, гороха, клевера, люпинов) возник очень удачный биоценоз (симбиоз) растений и бактерий. При этом последние могут восстанавливать непосредственно азот воздуха в аммиак. Клубеньковые бактерии используют для этого фермент нитрогеназу, содержащую молибден и железо.
В отличие от металлоферментов у других ферментов те же ионы металлов связаны непрочно. Они часто находятся далеко от активного центра. Однако ионы металлов повышают активность ферментов и поэтому называются активаторами. Вероятно, они придают ферментам более выгодную трехмерную структуру и стабилизируют эту оптимальную конформацию подобно "металлическому корсету". С помощью активаторов в организме может осуществляться прямое управление различными ферментативными процессами. Кроме вышеупомянутых микроэлементов многие ферменты активируются также марганцем, магнием, хромом, никелем, селеном и алюминием. Активность ферментов может также повышаться и регулироваться ионами электролитической среды клетки, такими, как ионы натрия, калия, кальция и хлора.
В последнее время получены данные об участии все большего числа микроэлементов в ферментативных реакциях. Но микроэлементы могут и подавлять активность ферментов. Например, ионы тяжелых металлов (ртути и свинца) являются опасными ядами почти для всех ферментов и, следовательно, для организма в целом.
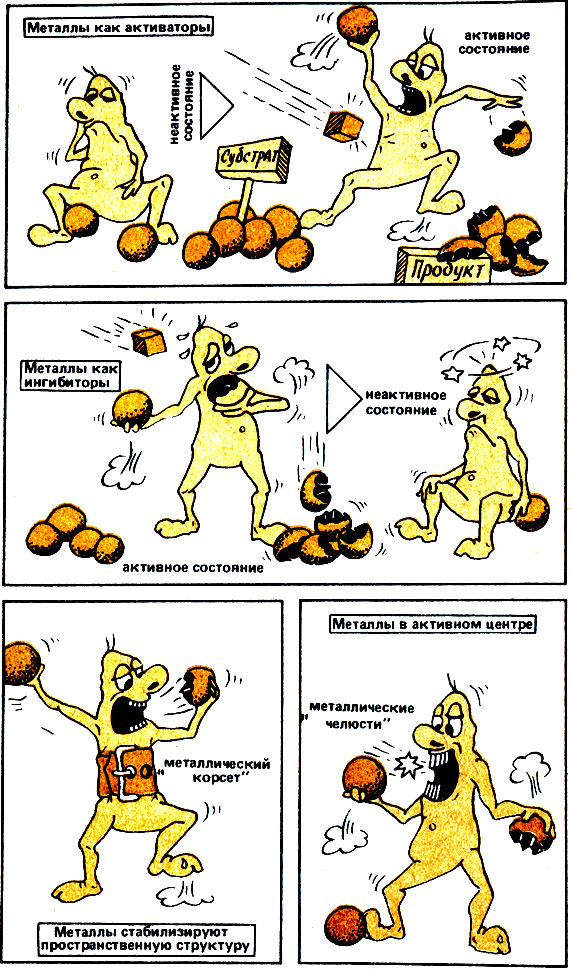
Рис. 7. Влияние металлов на ферментативные реакции. Металлы активируют или ингибируют ферменты, стабилизируют их пространственную структуру ('металлический корсет') или входят в состав активного центра ('металлические челюсти')
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'