
По дороге к "холодной" химии будущего
Ферментная технология-революция в промышленности
Промышленное применение ферментов и микроорганизмов с их ферментативными системами приведет к созданию абсолютно новой отрасли химической промышленности, которая будет приобретать в будущем все большее значение. Это позволит во многих случаях заменить технологии, в которых сегодня используются высокое давление и высокие температуры, на ферментно-технологические процессы, протекающие при нормальной температуре и давлении и позволяющие поэтому существенно снизить потребление энергии. С помощью ферментной технологии на основе принципиально новых методов удастся, по-видимому, получать ряд сложных продуктов, синтез которых ранее был просто невозможен или затруднен, поскольку он вызывал сильное загрязнение окружающей среды и был очень энергоемким.
На конгрессах и симпозиумах последних лет с участием видных представителей мировой науки наметились перспективные направления и задачи в области использования ферментов:
создание предпосылок для использования мультиферментных систем (разработка методов иммобилизации, стабилизации и регенерации кофакторов*);
* (Под кофакторами понимают коферменты и важные для протекания ферментативных реакций низкомолекулярные вещества (например, ионы).)
использование ферментов в качестве промышленных катализаторов для синтеза высокоочищенных продуктов, биологически активных веществ, чистых химических реактивов и принципиально новых соединений;
использование "обратной" ферментативной реакции и неизученных (новых) каталитических активностей, биокатализа в экстремальных условиях, например в органических растворителях вместо воды;
использование ферментов в качестве инструментов в генно-инженерных исследованиях;
улучшение свойств ферментов с помощью "белковой инженерии";
разработка химических моделей ферментативных реакций;
использование ферментов в медицинских целях, в том числе при пересадке искусственных органов;
разработка биосенсоров и ферментативных усилителей слабых сигналов;
получение энергии с помощью ферментов (получение водорода, а также культур клеток, которые могут служить биологическими источниками энергии).
Большие возможности ферментной технологии будущего демонстрирует уже сегодня изящный ферментативный метод, разработанный в Калифорнии С. Л. Нейдлменом и сотр. (фирма "Цетус корпорейшн"). Речь идет о ферментативном синтезе оксидов алкенов, производство которых в промышленном масштабе должно быть освоено уже к концу 80-х годов. Ожидается, что прибыль от реализации продукции этого и других аналогичных биотехнологических процессов составит 2-3 млрд. долларов в год.
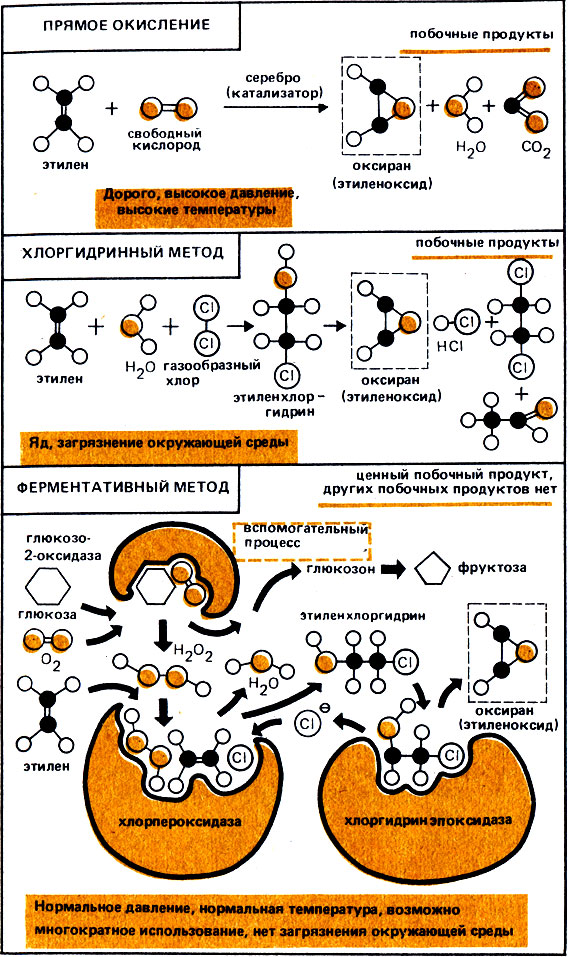
Рис. 34. Способы синтеза алкеноксидов из алкенов на примере этилена. Вверху - обычный химический способ. Внизу - ферментативный способ, разработанный 'Цетус Корпорейшн'
Алкеноксиды, т.е. оксиды ненасыщенных углеводородов с короткой цепью, имеющие двойную связь между двумя атомами углерода, широко используются как сырье в производстве пластмасс, пластификаторов, лакокрасочных покрытий и клеев. Сейчас алкеноксиды получают путем химического синтеза из газообразных алкенов нефти, например из этилена, пропилена (рис. 34). Прямое окисление, протекающее при температуре 240-260°С, давлении в 20 атмосфер с использованием серебра в качестве катализатора и с потреблением чистого кислорода, является дорогостоящим и энергоемким. В другом химическом производстве (где промежуточно получают хлоргидрин) используется газообразный хлор, который ядовит (следовательно, необходимы дополнительные затраты на соблюдение требований техники безопасности!) и его производство связано с большими затратами энергии. При химических процессах образуются нежелательные отходы и трудноотделимые побочные продукты.
При ферментативном способе используются в свободной или иммобилизованной форме три оксидоредуктазы микроорганизмов (хлорпероксидаза, хлоргидринэпоксидаза и глюкозо-2-оксидаза). Биотехнологический процесс протекает при нормальных температуре и давлении. Источником хлора при хлорировании алкенов служит обычная поваренная соль (хлорид натрия). Высвобождающиеся при этом ионы хлора используются в процессе повторно, причем в отличие от химического способа не загрязняется окружающая среда. Процесс не сопровождается образованием нежелательных побочных продуктов. Напротив, фруктоза, образующаяся в H2O2-генерирующем побочном процессе, - это очень нужный сахар (см. выше). Несмотря на то что пока не опубликованы экономические показатели этого биотехнологического процесса, уже сейчас можно прогнозировать его использование, основываясь только на вышеуказанных преимуществах. Однако последнее слово и здесь остается за практикой - "пробным камнем" истины.
При получении новых сложных продуктов, по-видимому, должны также привлекаться не менее сложные ферментативные системы и реакции. В двух предыдущих главах мы познакомились с некоторыми примерами применения ферментов в медицине и промышленности в настоящее время. В большинстве случаев это гидролитические ферменты, не требующие никаких вспомогательных систем в форме кофакторов (коферменты и ионы). "Простые" растворимые ферменты условно называют ферментами первого поколения, те же самые ферменты, но в иммобилизованной форме - вторым поколением. К третьему поколению относят иммобилизованные мультиферментные системы, функционирующие с помощью кофакторов. При применении ферментов третьего поколения возникает ряд новых проблем. Ведь соответствующие ферменты этих мультиферментных систем должны быть синтезированы, выделены и очищены. Осуществить уже одно это в крупных промышленных масштабах трудно, поскольку внутриклеточные ферменты, как правило, плохо "переносят" очистку и часто бывают очень нестабильными. Поэтому после получения для стабилизации их иммобилизуют с помощью оптимальных методов. Другим препятствием на пути использования ферментов третьего поколения является зависимость их функционирования от кофакторов. В ферментативной реакции кофакторы (например, НАДФ, НАДФ-Н*. АТФ, ионы) "потребляются" как субстраты. Поскольку их получение связано с большими затратами средств и труда, единственным экономически реальным выходом является их повторная регенерация с помощью химических, биохимических или электрохимических реакций. Многие ферментативные процессы не удалось до сих пор внедрить в промышленность именно из-за отсутствия удобных методов регенерации. Известный французский специалист в области ферментной технологии проф. Д. Тома, работающий в Компьенском университете, считает, что страна, в которой будет найдено и запатентовано практическое решение проблемы регенерации кофакторов, таких, как АТФ или НАДФ-Н, будет иметь большое (стратегическое) преимущество перед всеми остальными странами.
* (НАДФ и НАДФ-Н-это восстановленные формы никотинамидадениндинуклеотида (НАД) и никотинамидадениндинуклеотидфосфата (НАДФ).)
Элегантный способ регенерации кофактора, основанный на использовании ферментного мембранного реактора, разработан К. Вандреем, М. Кула и Ф. Бюкманном (ФРГ). Реактор используется для промышленного синтеза дорогостоящих аминокислот (таких, как L-лейцин и L-аланин) из кетокислот с помощью НАД-Н-зависимых дегидрогеназ. При постоянной работе реактора в течение 90 суток каждая молекула дорогостоящего НАД-Н регенерирует 70000-90 000 раз из НАД под действием формиатдегидрогеназы при использовании формиата в качестве субстрата. Формиат - дешевое и легкодоступное вещество, и ни он, ни продукт реакции CO2 не мешают работе фермента. Для того чтобы предотвратить утечку кофакторов через мембрану, его ковалентно иммобилизуют на водорастворимых полимерах, которые по размерам в 100 раз превышают кофактор.
Однако некоторые скептики считают, что вне клетки принципиально невозможны успешная стабилизация, регенерация кофакторов и эффективное функционирование мультиферментных систем. Для таких сложных реакций в общем случае надо использовать иммобилизованные клетки (см. выше); Обнадеживает, однако, что с помощью иммобилизованной мультиферментной системы грамицидин-S-еинтетазы удалось синтезировать антибиотик грамицидин S, применяя АТФ- генерирующую ферментативную систему. Тем самым было показано, что и вне клетки возможен эффективный синтез биологических соединений с помощью мультиферментных систем. Однако успешные лабораторные опыты еще далеко не означают, что этот метод может быть также применен в крупных промышленных масштабах.
Целенаправленный ферментативный синтез сложных биологически активных веществ, таких, как антибиотики, витамины, простагландины, нейропептиды и кофакторы, станет важной отраслью ферментной технологии будущего. По-видимому, будут открыты и совершенно новые области применения ферментов. Так, например, с помощью ферментов можно производить ароматические душистые вещества или можно устранить нежелательный привкус у определенных продуктов (из рыбы или соевых бобов).
Интересным направлением ферментативного синтеза, получившим развитие лишь в последние годы, является "обращение" ферментативного катализа. Заметим, что в случае ферментативных реакций речь всегда идет о равновесных, т.е. обратимых, реакциях. Например, если в "нормальных" условиях фермент "гидролизует" субстрат на два продукта (прямая реакция), то при изменении условий реакции тот же фермент может вновь "соединить" продукты гидролиза (обратная реакция). Следовательно, гидролазы можно использовать не только для расщепления субстратов, но и для синтезов. Пенициллин-амидаза расщепляет пенициллин в щелочной среде в прямой реакции на 6-аминопенициллановую кислоту и соответствующую боковую цепь (см. выше). Однако в кислой среде тот же фермент в обратной реакции вновь соединяет 6-аминопенициллановую кислоту и боковую цепь. Следовательно, для получения модифицированных синтетических пенициллинов достаточно просто с помощью пенициллинамидазы, действующей в обратной реакции, соединить пенициллановую кислоту с нужной новой химически полученной боковой цепью. Сходным образом с помощью протеаз можно получить новые белки из аминокислот.
Инсулин человека и свиньи различается лишь по одной N-концевой аминокислоте: в одном случае аланин заменен на треонин. Однако такое минимальное различие в белке вызывает у некоторых больных диабетом при введении инсулина свиньи нежелательные иммунологические реакции. Наряду с инсулином человека, который получают методами генной инженерии с использованием бактерий, некоторые фармацевтические фирмы продают инсулин свиньи, который с помощью фермента превращен в гормон человека. Для замены аланина на треонин используется "обратная" реакция протеазы трипсина, которая идет в присутствии органических растворителей.
Новый синтетический дипептид аспартам, который в 200 раз слаще, чем сахар, начала производить японская фирма "Тойо сода", используя для синтеза "обратную" реакцию протеазы термолизина, при которой происходит конденсация двух аминокислот (аспарагиновой и метилового эфира фенилаланина) с образованием дипептида.
Перспективно также использование ферментов не в водных растворах, как обычно, а в органических растворителях. Тем самым можно избежать нежелательных гидролитических реакций, а также удается подвергнуть ферментативному превращению труднорастворимые в воде вещества.
Хорошо известно, что для работы фермента нужна вода, однако А. Клебанов (Массачусетский технологический институт, Кембридж, США) показал, что ферментативная реакция может протекать с высокой эффективностью и в органических растворителях, содержащих менее 1% воды, если фермент иммобилизовать на носителе, который удерживает воду в окружении фермента. Это используется для этерификации жиров с помощью липазы, растворенной в органических растворителях. Такая липаза обладает поразительной стабильностью даже при 100°С
Клебанов также предложил проанализировать все известные коммерческие препараты ферментов для того, чтобы выявить в них новые каталитические активности. Так, было установлено, что глюкозооксидаза не обладает абсолютной специфичностью к кислороду косубстрата. Бензохинон может с успехом заменить O2. В результате такой реакции образуется важное химическое соединение гидрохинон, причем почти со 100%-ным выходом.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'