
4. Боковые ветви обмена углерода
Как боковые ветви обмена углерода, заканчивающиеся биосинтезом и накоплением специфических веществ экологического или структурного назначения, могут функционировать и основные пути обмена, при условии блокирования дальнейшей трансформации промежуточных продуктов биосинтеза, накапливающихся в клетке или в культуре. Примером этого может служить накопление этилового алкоголя у дрожжей (спиртовое брожение) или молочной кислоты у мукоровых грибов или, наконец, маннита у видов рода Aspergillus. В основе этих боковых путей углеродного обмена лежит всего один дополнительный этап, состоящий в восстановлении образующихся метаболитов и отвлекающий эти продукты из путей основного обмена.
Однако существуют специальные многоэтапные боковые пути биосинтеза, отобранные в процессе эволюции как важные экологические приспособления. Особенно много таких приспособительных биосинтезов существует в путях обмена жиров и терпенов. Как тот, так и другой пути исходят в основном из ацетата или, вернее, из ацетил-КоА.
Обмен жиров и образование полиэнов. Жирные кислоты и жиры имеют наиболее близкое отношение к основному обмену, так как являются структурными элементами клетки, обеспечивающими сохранение раздела сред почти во всех мембранных клеточных структурах (клеточные мембраны, митохондрии, аппарат Гольджи и т. д.). Видимо, липиды, а в особенности стероиды и фосфолипиды, являются не только запасными веществами, хотя и эту роль они тоже играют, а составляют компоненты структурных элементов клетки, обеспечивая определенные механизмы проницаемости, последовательность биохимических реакций и поддержку определенной структурной организации клеточных элементов. Особое значение они имеют для функционирования многочисленных мембранно-связанных энзимов.
Липиды занимают очень важное место в обмене грибов, это можно видеть уже из данных по их общему количеству (Weete, 1980), которое, с одной стороны, может достигать больших величин от сухой массы, а с другой - может сильно колебаться в зависимости от внешних условий и возраста культуры.
Особенно большие количества липидов находили у ряда мукоровых грибов (до 40-55%), у дерматофитов (45-56%), у некоторых рас дрожжей (до 65-87%) и у Chaetomium gtobosum (54%). То, что при отдельных анализах их количество сильно меняется, например, у Claviceps purpurea в 15 раз, а у Tilletla nudus более чем в 200 раз и почти у всех мукоровых грибов в 10 раз, указывает на очень активное участие липидов в их обмене веществ, сопровождающееся либо их синтезом, либо распадом.
В составе липидов грибов и других организмов обычно различают шесть фракций: углеводороды, стеролы, их эфиры, жирные кислоты, их глицериды и фосфолипиды, среди которых наиболее мощные фракции у грибов составляют триглицериды жирных кислот и фосфолипиды (Weete, 1980).
У отдельных таксономических и экологических групп соотношение фракций может меняться (табл. 3.2). Например, почти у всех дрожжей более важное место по сравнению с триглицеридами занимают эфиры стеролов, тогда как у исследованного представителя оомицетов Pythium ultimum фосфолипиды уступают место свободным жирным кислотам (см. табл. 3.2).
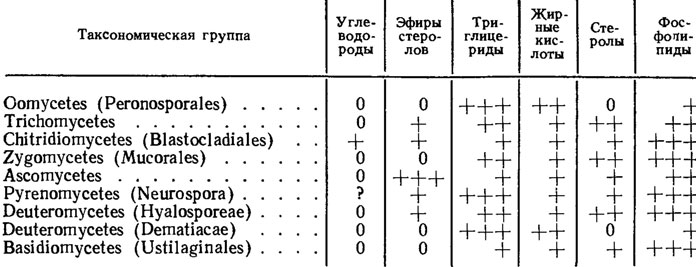
Таблица 3.2. Сравнение фракционного состава липидов грибов из разных таксономических групп (+++ - 30-60%; ++ - 10-30%; + - 10%)
Принципиальная схема биосинтеза насыщенных жирных кислот исходит из малоновой кислоты, точнее из малонил-КоА, образующегося из ацетил-КоА путем включения в него СО2, происходящего аналогично образованию щавелевоуксусной кислоты из пировиноградной. В этой реакции также участвуют биотин и используется энергия фосфорных связей, получаемая от АТФ. Во всех реакциях биосинтеза жирных кислот ведущую роль занимает КоА (рис. 3.8).
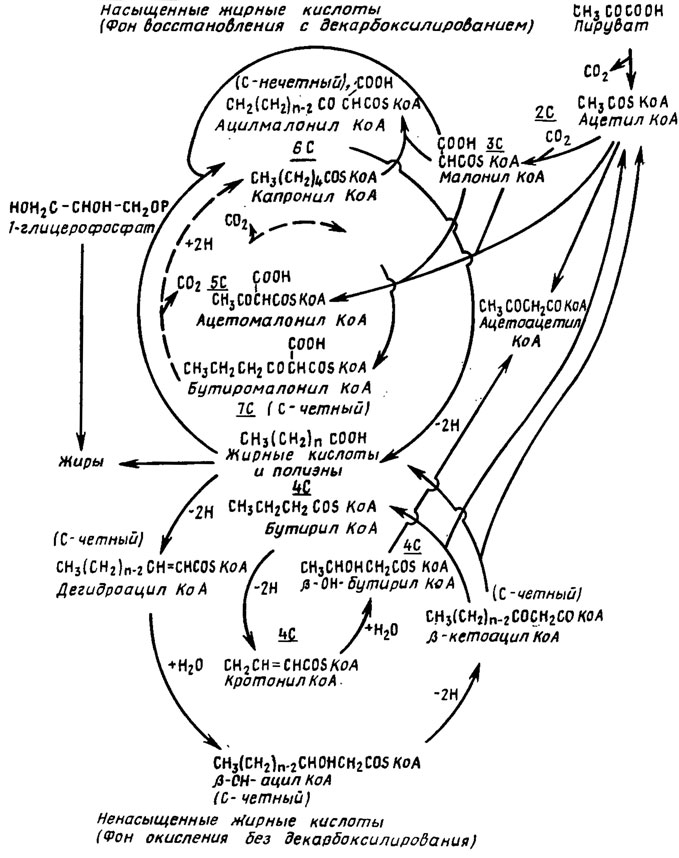
Рис. 3.8. Сопряженная схема биосинтеза насыщенных и ненасыщенных жирных кислот
Первый этап биосинтеза насыщенных жирных кислот состоит во включении СО2 в ацетил-КоА, в результате чего образуется малонил-КоА.
Во втором этапе происходит конденсация малонил-КоА с новой порцией ацетил-КоА, в результате чего синтезируется содержащий пять атомов углерода ацетомалонил-КоА.
Вслед за этим протекает третий этап - восстановление и декарбоксилирование ацетомалонил-КоА с образованием бутирил-КоА, содержащего уже четыре атома углерода. В этой реакции принимает участие НАДФ-Н.
Конденсация с малонилкоэнзимом А может повторяться боль шее число раз, каждый раз сопровождаясь декарбоксилированием и восстановлением, что приводит к добавлению на каждой ступени по два атома углерода к образующейся цепи жирной кислоты. Принимающие в этом процессе участие энзимы и кофакторы приведены в схеме на рис. 3.8, 3.9.
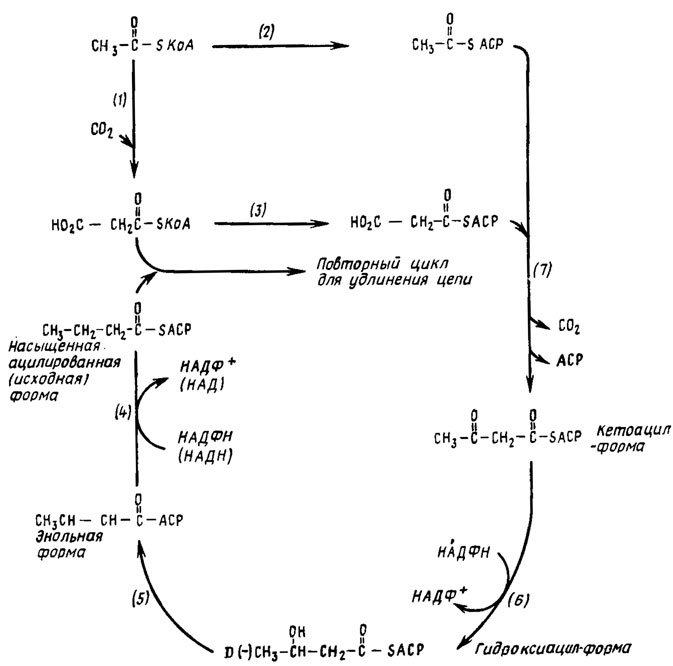
Рис. 3.9. Путь биосинтеза жирных кислот (Weete, 1980). SCoA - коэнзим А; SACP - переносящий ацильные группы протеин. Участвующие в синтезе жирных кислот энзимы: 1 - ацетил-КоА-карбоксилаза; 2 - ацетил-КоА-АСР-трансацилаза; 3 - малонил-КоА-трансацилаза; 4 - эноил-АСР-редуктаза; 5 - 3-гидрокси-АСР-дегидраза; 6 - 3-кетоацил-АСР-редуктаза; 7 - кетоацил-АСР-синтетаза
Образование насыщенных жирных кислот обычно происходит на фоне более восстановленного режима обмена, т. е. при относительно низком рН системы, тогда как насыщенные жирные кислоты требуют для биосинтеза большего преобладания процессов окисления, т. е. более высокого уровня рН и участия в биосинтезе окисленной формы НАД+. При этом ацилированная форма насыщенной жирной кислоты (R-СО-SKoA) отдает по второму и третьему атомам углерода два атома водорода и по этим атомам углерода образуется двойная связь. По ней может присоединяться с помощью энолгидразы молекула воды, образуя оксикислоту, которая при вторичном окислении НАД+-дегидрогеназой дает кетокислоту, способную отщеплять по кетогруппе фрагмент ацетил-КоА. Образующиеся в результате такого окисления и расщепления жирные кислоты обычно содержат на два атома углерода меньше в их цепи, чем исходные. Описанный процесс известен под названием β-окисления. Повтор первых двух этапов может привести к образованию полиенов и жирных кислот с высокими уровнями ненасыщенности. Этот процесс протекает в основном в митохондриях с участием карнитина в переносе через мембрану (рис. 3.10) ацилированных жирных кислот. Это хорошо согласуется с отмеченным ранее (Беккер, 1956, 1963) совпадением снижения количества жиров в мицелии продуцента пенициллина и других грибов с дифференцировкой клеточных структур, в частности с сильным обогащением митохондриями. Напротив, более ранний в их онтогенезе период накопления жиров характерен, судя по цитохимическим признакам, обилием в гифах микросомальной фракции.
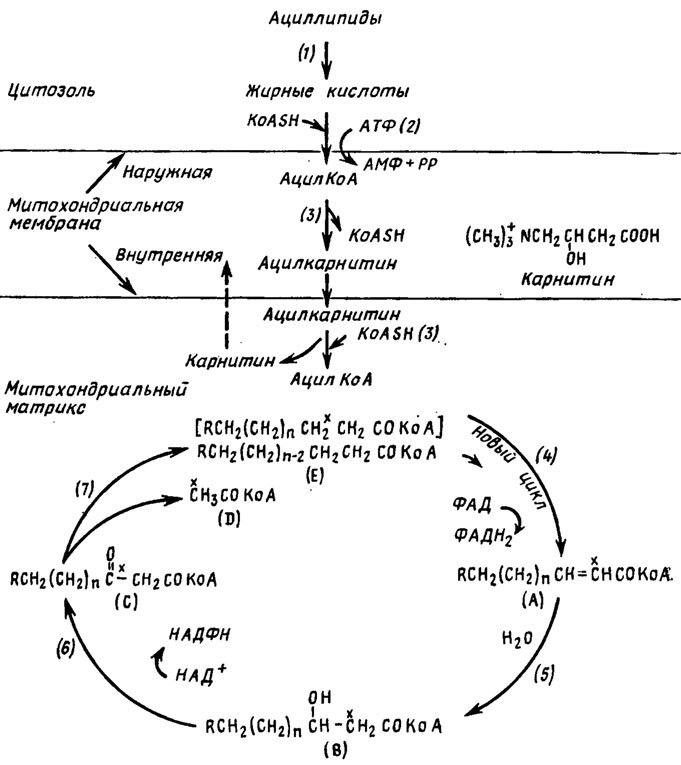
Рис. 3.10. Транспорт ацнльных еднннц через мнтохондриальную мембрану и в-окисление жирных кислот (по Weete, 1980). Промежуточные продукты: (А) - транс-Δ2-ацил-КоА; (В) - L(+)-β-гидроксиацил-КоА; (С) - β-кетоацил-КоА; (D) - ацетил-КоА; (Е) - ацил-КоА. Участвующие в транспорте энзимы: 1 - липаза; 2 - ацнлтнокнназа; 3 - ацил-КоА-карнитинтрансацилаза; 4 - ацилдегидрогеназа; 5 - эноилгндратаза; 6 - 3-гидроксиацилдегндрогеназа; 7 - 3-кетоацилтиолаза
Приведенное выше представление о ходе биосинтеза жирных кислот требует некоторых дополнений: во-первых, порядок очередности формирования жирных кислот в настоящее время трактуется как последовательность от кетоформы, через гидроксиформу и энольную, к насыщенной форме, а не наоборот (см. рис. 3.8). Обратный порядок приписывается не синтезу, а использованию жирных кислот. Во-вторых, у грибов обнаружен путь формирования ненасыщенных жирных кислот из насыщенных, который локализован в микросомальной фракции цитоплазмы и включает оксигеназную систему с участием цитохрома 450, весьма сходную с таковой у дрожжей (Weete, 1980). Порядок реакций в этой системе следующий:
НАДН → НАДН-цитохром b5 редуктаза → цитохром b5 → ЦЧФ →
→ пальмитил КоА + О2
↓пальмитолеил КоА + Н2О
(ЦЧФ - цианидчувствительный фактор)
Данные о сравнительных свойствах синтетаз жирных кислот у разных организмов (Weete, 1980) показали, что у грибов они ближе к синтетазам млекопитающих. Синтетазы как у животных, так и у грибов представляют собой не индивидуальные энзимы (как у бактерий и растений), а мультиферментные системы.
Распад жиров в клетках грибов происходит в более поздних стадиях онтогенеза либо при формировании из ненасыщенных жирных кислот низко молекулярных насыщенных фрагментов (Беккер, 1956, 1963), либо при полном их окислении с последовательным отщеплением двухуглеродных фрагментов ацетата, деградирующих в цикле трикарбоновых кислот до СО2 и воды. Распад этого типа (β-окисление) энергетически очень продуктивен, так как окисление каждого двухуглеродного фрагмента дает формирование пяти молекул АТФ, для начальной же активации этого процесса требуется только одна молекула АТФ.
Уравнение реакции трансформации жирной кислоты: Жирная кислота С18 + 1 АТФ + 8 KoASH + 7 ФАД + 7 НАД+ → 8 АцКоА + -7 ФАДН2 + 7 НАДН + 7 Н+ + АМФ + РРн (пирофосфат). Исходя из этого рассчитано, что при распаде одной молекулы пальмитиновой кислоты (жирная кислота C18) с последующим полным окислением восьми молекул ацетил-КоА в цикле ТКК получается выход 130 молекул АТФ на одну молекулу жирной кислоты, которые составляются из 21 моля АТФ в результате окисления восьми молей НАДН (3×7 НАДН), 14 молей АТФ при окислении ФАДН2 (2×7 ФАДН2), а также из 95 молекул АТФ от окисления восьми молекул АцКоА (12×8 АцКоА) - 1 АТФ на активацию. Выход энергии в калориях на 1 моль кислоты Cis равен 2330 ккал/моль, что дает КПД порядка 42% (Weete, 1980).
Сходным образом с жирными кислотами синтезируются, а подчас используются в обмене полиэны с большим количеством двойных связей, которые часто являются антибиотиками почвенных грибов или входят в их состав; например, кротоновая и декатетраэновая кислоты, входящие в состав антибиотиков трихотецина и фумагиллина, а также антибиотики палитантин и фреквентин.
Обычно особенно богаты жирами приспособления грибов, предназначенные для сохранения вида в экстремальных условиях температуры или при недостатке воды, как склероции или хламидоспоры. Это объясняется, с одной стороны, защитной ролью жиров в повышении стойкости к изменениям температуры и к потере влаги, а с другой - их функцией как энергетического и строительного резерва для биосинтезов при прорастании.
В связи с их важной функцией в составе клеточных мембранных структур липиды, в особенности их фосфолипидная фракция, в частности и у грибов, стали изучаться особенно детально. Исследован жирно-кислотный состав мицелия и плодовых тел около 200 видов грибов, данные о которых приведены в сокращенном виде в табл. 3.3.
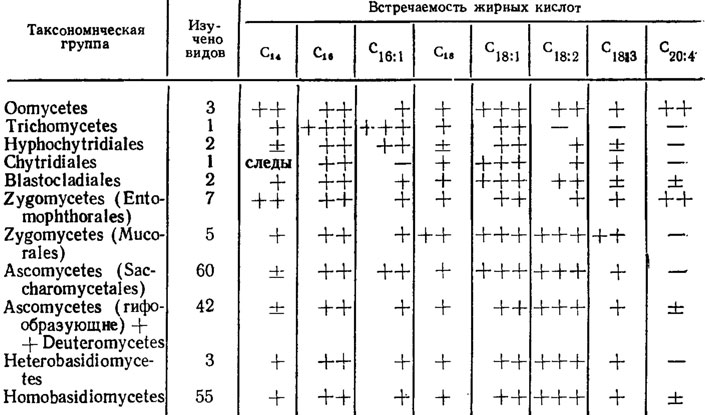
Таблица 3.3. Распространение жирных кислот в составе липидов грибов из различных таксономических групп (Weete, 1980) (+++) - 20-30% от суммы жирных кислот; (++) - 10-20%; (+) - 1-10%; (±) - данные расходятся у разных видов; (-) - отсутствует
Из результатов исследований, в табл. 3.3, можно извлечь в основном только довольно тривиальный вывод о преобладании у грибов вообще пальмитиновой и олеиновой кислот, а начиная с мукоровых грибов и выше в порядке их эволюции дополнительно линолевой и в меньшей мере линоленовой. Из кислот более высокомолекулярных приуроченностью к определенным группам грибов обладает кислота С20:4 (арахидоновая), присущая, видимо, оомицетам и с большей степенью достоверности энтомофторовым грибам класса зигомицетов (см. табл. 3.3), что может говорить о более позднем происхождении и экологической значимости жирных кислот высоких порядков молярности и ненасыщенности у грибов.
В связи с потребностью медицинской промышленности в простагландинах жирные кислоты с высоким числом атомов углерода, продуцируемые некоторыми грибами, привлекли особое внимание как возможное сырье для изготовления этих препаратов. Предшественником простагландинов, осуществляющих регуляцию хода воспалительных и аллергических процессов и стимулирующих активность фермента, синтезирующего циклический АМФ, аденилатциклазу, которые имеют очень различную направленность действия в зависимости от типа, является 5,8,11,14-эйкозотетраэновая, или арахидоновая кислота (рис. 3.11). В связи с проблемой ее биосинтеза у ряда грибов состав липидов изучался в последние годы более подробно. В научной литературе опубликовано много материалов на эту тему. В частности, изучались грибы из класса зигомицетов (мукоровые и энтомофторовые) и некоторые несовершенные грибы со своеобразной экологией нематофагов или микопаразитов.
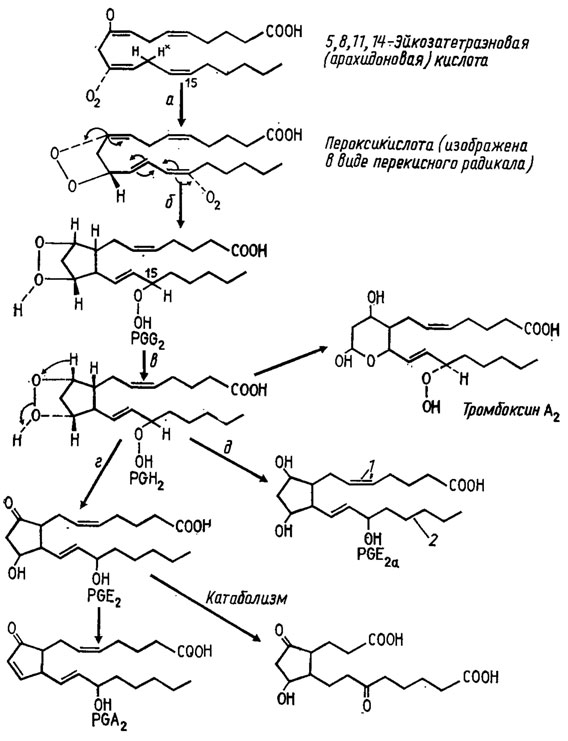
Рис. 3.11. Биосинтез простагландинов и некоторые реакции их распада: а - реакция сходная с действием липооксигеназы, в ходе которой происходит отщепление протона (Н+) у С-13; б - формирование простагландина G2; в, г, д - формирование соответственно простагландинов Н2, Е2 и Е2а; д - восстановительное расщепление перекиси. Стрелки при PGE2a: 1 - в простагландинах ряда 1 эта двойная связь отсутствует; 2 - в простагландинах ряда 3 присутствует еще одна двойная связь (Мецлер, 1980)
У хорошо освоенного в промышленных условиях продуцента каротиноидов Blakeslea (Choanephora) trispora липиды представлены в основном триглицеридами и несколько в меньшей степени суммарной фракцией фосфолипидов и моноглицеридов, дополняемых позднее формирующимися стеролами и свободными жирными кислотами (Дедюхина, Бехтерева, 1968). Состав их характеризуется обилием пальмитиновой, стеариновой, олеиновой, линолевой и линоленовой кислот, с некоторым преобладанием насыщенных кислот над ненасыщенными. В культуре на глюкозе количества последних со временем увеличивается, чего не происходит в культуре с добавкой n-гексана (Бехтерева и др., 1969). Среди жирных кислот, находящихся в составе фосфолипидов В. trispora, есть различия между культурами разного пола (+ и - штаммами). Например, олеиновой кислоты больше у штамма (+), тогда как линолевой у штамма (-), хотя степень насыщения суммы жирных кислот у обоих штаммов примерно равна, а в смеси их в 3 раза выше. Качественный их состав близок к общим липидам, но несколько уже и не включает представителей с наиболее короткой (C12) и наиболее длинной (С20) цепью.
Образование липидов у В. trispora оказывается до некоторой степени коррелирующим с синтезом каротиноидов (табл. 3.4), что, возможно, связано с их общим происхождением из ацетил-КоА (рис. 3.10 и 3.12), хотя возрастание последних в зависимости от содержания сахара в среде намного превосходит возрастание концентрации общих липидов и триглицеридов (Дедюхина, Бехтерева, 1969).
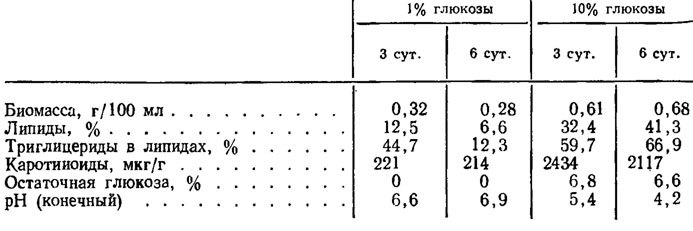
Таблица 3.4. Биомасса, липиды и каротиноиды в мицелии Blakeslea trispora при росте на среде с различной концентрацией глюкозы (Дедюхина, Бехтерева, 1969)
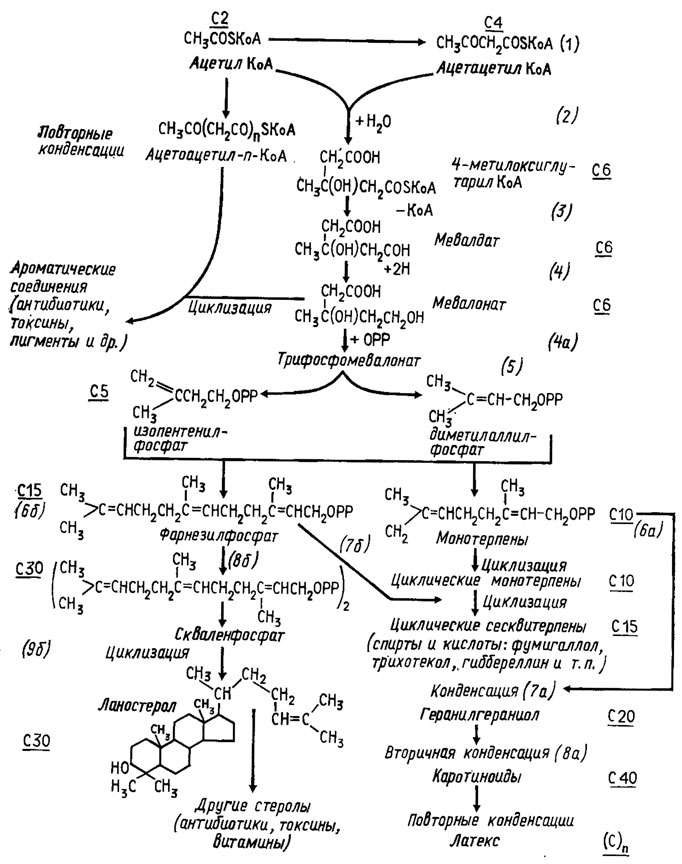
Рис. 3.12. Схема обмена терпенов (Miller, 1961), модифицированная и дополненная применительно к грибам
Исследование жирно-кислотного состава фосфолипидов двух видов мукоровых грибов из того же, что и Blakeslea семейства Choanephoraceae, а именно Cunninghamella elegans и С. homotallica, показало сходные с фосфолипидами Blakeslea trispora результаты. В обоих случаях ведущими в составе фосфолипидов оказались пальмитиновая, олеиновая и линолевая кислоты, в стабильно близкой концентрации включались пальмитолеиновая и стеариновая. Коэффициент насыщения, показывающий преобладание примерно в три раза ненасыщенных форм, был почти идентичен у всех трех видов. Единственными отличиями видов рода Cunninghamella оказались стабильное присутствие у них от 7 до 12% линоленовой кислоты и расширение качественного состава жирных кислот, в особенности в сторону высокомолекулярных, вплоть до содержащих 24 атома углерода в цепи (Бехтерева, Яковлева, 1980).
Своей специфичностью сильно отличается от жирно-кислотного состава мукоровых грибов аналогичный состав общих липидов видов рода Entomophthora, растущих на синтетической среде с бактопептоном и дрожжевым экстрактом, что исключает заимствование состава от насекомых, на которых они обитают в природе (Попова и др., 1980).
Он оказался очень разнообразным, включая для вида Entomophthora thaxteri 26 жирных кислот с размером цепи от 9-углеродной до 24-углеродной, против 13, установленных у Blakeslea trispora. Он характерен обилием низкомолекулярных кислот типа лауриновой и миристиновой, в ущерб пальмитиновой и стеариновой, и обилием высокомолекулярных (С18-С20) ненасыщенных жирных кислот с различно расположенными двойными связями, это, в общем, снижает степень насыщенности их суммы.
Кроме всего этого особенно обращает на себя внимание наличие у них разветвленных (изоформ) жирных кислот и обилие доходящей до 10% состава у Е. thaxteri высоконенасыщенной (С20:4) арахидоновой кислоты, что характерно для липидов некоторых животных, в частности для червей - гельминтов (Soprunov, 1978).
В процессе развития культур Entomophthora количество (в зависимости от вида) различных жирных кислот имеет таксономическое значение, хотя наиболее высокомолекулярные (C18, С20:4) сохраняются в течение вегетации на мало изменяющемся уровне (Попова и др., 1980). Жирно-кислотный состав фосфолипидов двух видов Entomophthora сходен с составом их в общих липидах этого рода и в нем также обильны миристиновая и пальмитиновая кислоты, хотя качественный состав компонентов уже (23 жирных кислоты вместо 29 в общих липидах). Присутствуют также разветвленные изоформы жирных кислот, а количество арахидоновой кислоты (С20:4), возможно важной для снижения ригидности клеточных мембран хозяев этих паразитных грибов, доходит к концу роста до 13-18% общего состава. Судя по уровню коэффициента насыщения ненасыщенность фосфолипидов у этого рода еще более выражена, чем в случае жирно-кислотных компонентов общих липидов. Состав жирных кислот фосфолипидов у исследованных видов сходен, за исключением большого преобладания у Е. conica пальмитолеиновой кислоты (20-23% С16:1).
Из числа дейтеромицетов исследовался состав общих липидов четырех видов (в числе пяти штаммов) хищных грибов из рода Arthrobotrys, специализированных на залавливании нематод (Раджабова и др., 1980). Фракционный состав этих липидов довольно закономерно отличается в зависимости от используемой для их выращивания среды, причем, хотя на среде Мейзе с глюкозой количество их оказывается большим, чем на среде Стефанини с сахарозой, количество фосфолипидов при росте на последней возрастает в 2-3 раза. У всех видов Arthrobotrys на обоих средах в составе липидов обильно представлены триглицериды (от 25 до 80%) и стеролы (до 12%). Последние являются компонентами биогенеза терпенов, продукты которого, видимо, участвуют в форме латексов и токсинов в актах хищничества грибов этого рода (Беккер, 1972). Жирно-кислотный состав общих липидов, в котором преобладают пальмитиновая, олеиновая и линолевая кислоты, относительно узок, что, как и в случае Blakeslea trispora, можно объяснить конкуренцией этого пула с шунтом терпенов (Arthrobotrys, как и Blakeslea, синтезирует каротиноиды и, кроме того, много других веществ, формирующихся по этому пути).
Также относительно узок жирно-кислотный состав общих липидов у продуцента сесквитерпенового антибиотика трихотецина, формирующегося также в шунте терпенов, микопаразита Trichothecium roseum. Однако его отличает обилие накапливающихся одновременно с антибиотиком на третий-четвертый дни культивирования высокомолекулярных сильноненасыщенных жирных кислот, в частности арахидоновой, количество которой не уступает обнаруживаемому у Entomophthora (Зеленева и др., 1979).
При сравнении жирно-кислотного состава фосфолипидов актиномицетов и грибов (Ковальчук и др., 1980) обнаруживается сходство по содержанию пальмитиновой, пальмитолеиновой и олеиновой кислот. Отличие состоит в меньшем диапазоне вариаций в числе атомов углерода в цепи у актиномицетов, в большей насыщенности жирных кислот и обилии их с нечетным числом атомов углерода в цепи.
По проценту жирных кислот с нечетным числом атомов углерода в цепи особенно сильно отличаются от актиномицетов сапрофитные мукоровые грибы родов Blakeslea и Cunninghamella, в фосфолипидах которых они полностью отсутствуют, что указывает на преобладание у них обычного пути синтеза и деградации жирных кислот с участием ацил-КоА. Напротив, наличие жирных кислот с нечетным числом атомов углерода указывает на изменения путей их биосинтеза со включением малоната без дальнейшего декарбоксилирования (см. рис. 3.8). Сближение в этом отношении с актиномицетами возможно для паразита насекомых Entomophthora и хищного гриба Arthrobotrys, но насыщенность жирных кислот, обеспечивающая им более свободное функционирование мембранно-связанных ферментов, у грибов выше. Необходимо отметить, что наиболее высокомолекулярные и сильноненасыщенные жирные кислоты (например, арахидоновая) встречались исключительно у мико- или энтомопаразитов (Trichothecium и Entomophthora), а также у некоторых паразитов растений из числа оомицетов, как Pythium и Phytophthora (см. Weete, 1980).
Как уже упоминалось выше, особенно важную структурную роль липиды, в том числе и жирные кислоты, играют в строении клеточных мембран, как ограничивающих клетку в целом, так и ее вакуоли и митохондрии. Данных в этом направлении, касающихся грибов, пока немного и они ограничиваются примерами из числа дрожжей. Жирно-кислотный состав плазмалеммы и митохондриальных мембран близок и, как и в общих липидах, характерен преобладанием пальмитиновой, олеиновой, а также пальмитолеиновой кислот.
Однако главным определяющим свойства различных мембран компонентом являются не столько жирные кислоты, сколько их сочетания с другими компонентами фосфолипидов, в частности с холином в фосфатидилхолине (PC), с этаноламином в фосфатидилэтаноламине (РЕ), с инозитом в фосфатидилинозите (PI), с серином в фосфатидилсерине (PS) и с дифосфатдиглицерином в кардиолипине (CL). Все эти формы фосфолипидов встречаются у грибов, и сочетания их в структуре плазмалеммы и тонопласта отличаются много сильнее, чем жирно-кислотный состав (табл. 3.5).

Таблица 3.5. Состав плазмалеммы и тонопласта Saccharomyces cerevisiae (по Weete, 1980)
* (Фосфолипиды выражены как процент липидного фосфата.)
Прежде всего липидов в тонопласте примерно в 2 раза больше, чем протеина, тогда как в плазмалемме отношение обратное. Основной фон в липидах мембран составляют не фосфолипиды, а стеролы, превышающие по молярности фосфолипиды, особенно в плазмалемме в 3-9 раз. Главным из них, особенно в плазматической мембране, является эргостерин. По составу отдельных фосфолипидов в клеточной мембране и тонопласте тоже имеются различия, вероятно, имеющие отношение к различиям в их функциях. Например, в плазмалемме отсутствует лизофосфатидилхолин, тогда как только в ней обнаруживается фосфатидная кислота.
При общем анализе фосфолипидных компонентов у грибов из различных таксономических групп выявляется общее правило обилия во всех их группах PC и РЕ. В группах сумчатых и высших базидиальных грибов учащаются встречи реже наблюдаемых у низших грибов PS и PI, тогда как у дрожжей почти в равной мере с ними представлен и CL. Отмечается также не только качественное, но и количественное сходство в наборе фосфолипидов, например у всех близких к роду Saccharemyces дрожжей, у представителей родов Fusarium и Cephalosporium.
Состав фосфолипидов разного типа в плазмалемме, митохондриях, микросомах и тонопласте дрожжей и в респираторных частицах спорыньи, приведенный в табл. 3.6, показывает наиболее широкое разнообразие этих компонентов в митохондриях и наиболее узкое в составе PC, РЕ и PI в тонопласте. Постоянно преобладают во всех фракциях мембран PC, РЕ и PL Структурная роль стеролов, в особенности эргостерина, пути биосинтеза которого излагаются ниже, несомненно очень велика для мембранных образований, так же, как и роль мембранных белков, которая, к сожалению, еще недостаточно изучена.
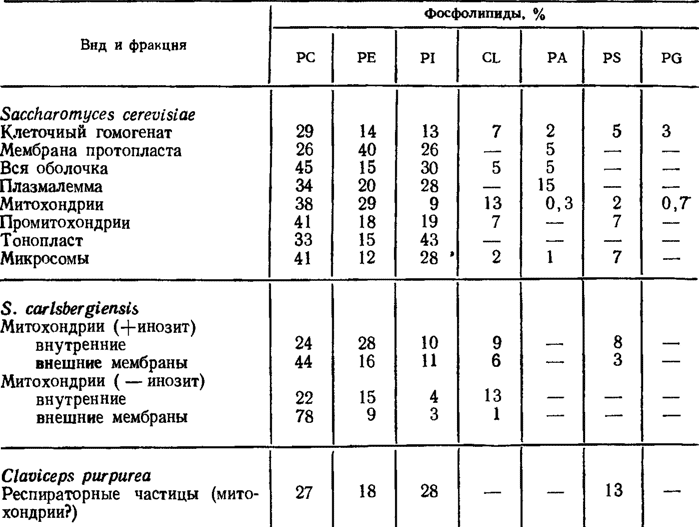
Таблица 3.6. Состав глицерофосфолипидов субклеточных фракций Saccharomyces cerevisiae, S. carlsbergiensis и Claviceps purpurea (Weete, 1980)
Примечание. РА - фосфатидная кислота, PG - фосфатидил глицерин, PC - фосфатидилхолин, РЕ - фосфатидилэтаноламин, PL - фосфатидилинозит, CL - кардиолипин, PS - фосфатидилсерин.
Синтез терпенов и ароматических соединений
Шунт терпенов у грибов особенно часто несет функции обмена с экологическим назначением, так как в нем синтезируется особенно большое количество соединений типа антибиотиков, токсинов, пигментов и других веществ с конкурентной, агрессивной (у паразитов) и защитной функцией. Этот путь биосинтеза начинается с ацетилкоэнзима А как и биосинтез жиров (см. рис. 3.12/Мiller, 1961), в частности с образования, при конденсации двух молекул ацетил-КоА, ацетоацетилкоэнзима А, т. е. четырехуглеродного продукта из двух, содержащих по два атома углерода. Во втором этапе этого пути биосинтеза происходит повторная конденсация ацетоацетил-КоА с ацетил-КоА с образованием шести-углеродного соединения, метилоксиглутарил-КоА. Утрачивая в дальнейшем связь с коэнзимом А, это соединение трансформируется в мевалдовую кислоту, содержащую кроме карбоксила еще я альдегидную группу.
В четвертом этапе биосинтеза терпенов это соединение восстанавливается с образованием мевалониевой кислоты, у которой альдегидная группа мевалдата заменена спиртовой. Одновременное наличие у мевалоната спиртовой гидроксильной и карбоксильной групп наделяет это соединение способностью к дальнейшим процессам циклизации и конденсации. В результате этого оно часто является исходным пунктом для дальнейших биосинтезов многих циклических соединений типа антибиотиков, пигментов и других, которые образуются при конденсации его с содержащими различное число атомов углерода фрагментами ацил-А.
Однако основной путь биосинтеза обычно приводит к фосфорилированию мевалоната, который в следующем, пятом, этапе этого метаболизма декарбоксилируется, трансформируясь в изолентенилфосфат или диметилаллилфосфат, содержащие по пять атомов углерода каждый и имеющие структуру, характерную для изопренов. В дальнейшем биосинтез может идти по двум альтернативным путям, но постоянно при участии фосфорилирования. Один из путей состоит в конденсации этих двух соединений в десятиуглеродную цепь алифатического или циклического строения. Соединения этого типа после их дефосфорилирования оказываются летучими и обладают сильно выраженным ароматическим запахом, входя в состав эфирных масел высших растений. Такие ароматические соединения, видимо, встречаются также и у многих грибов, например у хищных грибов из рода Arthrobotrys (Беккер, 1972).
Такие соединения с десятиуглеродным строением носят название монотерпенов и могут конденсироваться далее с образованием дитерпенов, содержащих двадцать атомов углерода (или четыре изопреновых фрагмента). Примером дитерпенов может служить геранилгераниол, который считается основным предшественником каротиноидных пигментов, широко представленных у грибов (Гудвин, 1954). Образование геранилгераниола и каротиноидов, видимо, также происходит за счет использования энергии фосфорных связей, дающих возможность конденсации до сорока атомов углерода каротиноидов, концевые группы которых могут далее циклизоваться с образованием α- и β-иононовых групп. Описан способ их формирования (Weete, 1980).
У целого ряда грибов, например у рода Lactarius из базидиомицетов и у хищных грибов нематофагов (Беккер, 1972), могут образовываться также латексоподобные вязкие и клейкие вещества, концентрирующиеся либо в клетках плодовых тел (у Lactarius), либо на поверхности ловчих колец мицелня (у хищного гриба Arthrobotrys и подобных ему видов).
По-видимому, такие вещества представляют собой изотерпеновые высокомолекулярные соединения, сходные по составу и биогенезу с латексом высших растений и образующиеся из моно- и димеров терпенов по этому же пути метаболизма. Как и латексы каучуконосов, они застывают на воздухе, превращаясь в вязкие и упругие резиноподобные вещества при их окислении. Их экологическое назначение еще не всегда понятно, однако в случае хищных грибов, залавливающих нематод, они несомненно принимают участие в акте хищничества.
Второй альтернативный путь биогенеза терпеновых соединений состоит в конденсации одной молекулы диметилаллилфосфата с двумя молекулами изопентенилфосфата с образованием пятнадцатиуглеродного соединения - фарнезилфосфата, дающего начала большому классу циклических терпенов, носящих название сесквитерпенов. Этот синтез так же, как и последующая конденсация двух молекул фарнезилфосфата в соединение с тридцатью атомами углерода - фосфорилированный сквален, происходит, как и ранее, при использовании энергии фосфорных связей. Дальнейшая циклизация сквалена приводит к образованию ланостерола, из которого образуются очень обильные и разнообразные у грибов циклические соединения из класса стероидов.
Следует отметить, что именно путь биосинтеза стеролов является одним из наиболее ярких биохимических признаков, отличающих грибы от растений и бактерий приближающих их обмен к животным. Это отличие наблюдается уже на первом этапе синтеза стеролов в момент циклизации сквалена (рис. 3.13), когда из сквалена 2,3-эпоксида в случае грибов и млекопитающих формируется ланостерол, а в организмах растений и у микроорганизмов - циклоартенол.
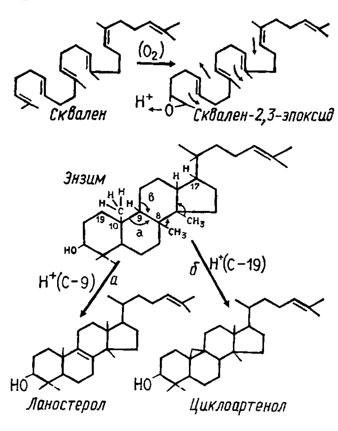
Рис. 3.13. Циклизация 2,3-сквалена с образованием ланостерола (у животных и грибов) или циклоартенола (у растений/Weete, 1980)
Принципиальные различия в ходе биосинтеза стеролов, в их групповом составе и происхождении у растений, животных и грибов заключаются в следующем.
Главным стеролом большинства грибов является принадлежащий к группе 4-десметил-С28-стеролов эргостерол, биосинтез которого идет через ланостерол, зимостерол, фекостерол и эргоста-3,24-диэнол:
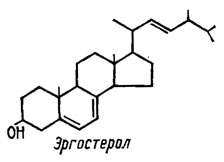
Эргостерол, являющийся у большинства грибов наиболее обильным и постоянным стеролом, сопровождаясь большей частью некоторыми другими стеролами из той же группы 4-десметил-С28-стеролов, отсутствует только у оомицетов из порядка Saprolegniales и у ржавчинных грибов (табл. 3.7). Возможно, что последние заимствуют характерные для них стеролы из группы стигмастерола у растений, на которых они произрастают. Однако такое предположение по поводу сапролегниевых грибов исключается. Здесь можно только, как и в случае их клеточной оболочки, почти целиком состоящей из целлюлозы, отнести факт отсутствия у них эргостерола к их иному происхождению, чем у грибов, синтезирующих хитин и эргостерин и тяготеющих к свойствам обмена, характерным для животных. В противоположность к ним оомицеты в части синтеза как полисахаридов, так и стеролов явно тяготеют к метаболизму, характерному для растений.
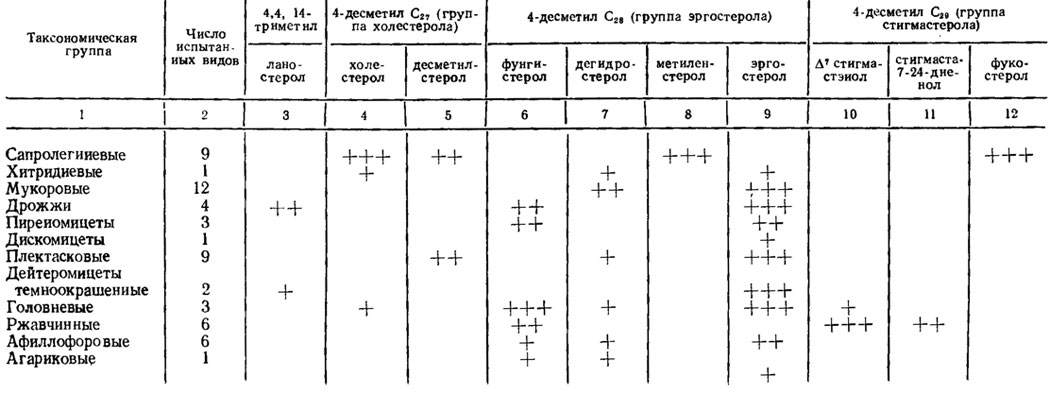
Таблица 3.7. Распространение преобладающих стеролов в различных таксономических группах грибов (Weete, 1980); обозначения: (+++) - 100%; (++) - ≥ 50%; (+) - 30-50% видов
Обе альтернативно формирующиеся в шунте терпенов группы циклических соединений - циклические спирты, образующиеся из фарнезола, и стеролы, производные сквалена и ланостерола, играют у многих грибов важнейшие экологические роли и обладают очень ярко выраженными различными видами биологической активности. Сесквитерпеновые спирты входят в состав противогрибных антибиотиков и токсинов, известных под общим названием трихотецеиов (трихотецина, роридина, триходермина, веррукарина/Кожибски и др., 1969; Беккер, 1972), а также антифаговых, протистоцидных (фумагиллин) и нематоцидных веществ (Беккер, Раджабова, 1972). Их содержат специфические индукторы роста и развития высших растений гормонального типа, продуцируемые грибами, например гибереллин.
Из числа стеролов помимо обильно продуцируемого грибами провитамина D - эргостерина, само название которому дали рожки спорыньи, грибы образуют антибиотики типа полипореновой кислоты у базидиомицетов, гельволевой кислоты у Aspergillus fumigatus, фуцидина у Acremonium fusidioides, розололактона у Trichothecium roseum и токсины, подобные токсинам Fusarium из секции Sporotrichiella (Олифсон, 1957).
Весь обмен терпеновых соединений обычно протекает на фоне низкого rН и поддерживается в условиях восстановления, в результате чего в процессе его лишь изредка образуются кислоты, а главным образом спирты и даже углеводороды, например летучие терпены, каротиноиды и латексы. Эта особенность приводит еще к одной важной экологической роли этих соединений. Они, например каротиноиды, нередко несут в обмене грибов функции антиоксидантов, предохраняющих их от избыточного окисления.
Подобную же роль противолучевых экранов и антиоксидантов играют, видимо, и синтезирующиеся по пути, сходному с синтезом стероидов или ароматических аминокислот, меланины (Allport, Bu'Lock, 1960; Жданова, 1976), распространенные у темноокрашенных сумчатых грибов и гифомицетов, у которых их ритм спорообразования регулируется светочувствительными факторами, например рибофлавином. Такой случай наблюдается у гифомицета Alternaria (Luckens, 1963).
Очень многие биологически активные вещества грибов относятся к ароматическим соединениям, производным бензола, нафтола и т. п. Относительно путей их образования существовал ряд гипотез, которые в последнее время свелись в основном к двум: 1) образование через шикимовую кислоту, изученное на бактериях и биохимических мутантах Neurospora crassa, и 2) через конденсацию производных и аналогов мевалониевой кислоты между собой или с ней самой, структура которой весьма пригодна для циклизации. Последний тип синтеза многократно изучался методом меченых атомов на очень многих видах грибов.
Биосинтез производных бензола (или фенола) через шикимовую кислоту идет следующим образом (рис. 3.14/Мiller, 1961). Происходит циклизация продуктов пентозного шунта обмена, вероятно исходя из стадии седогептулозы, которая приводит к образованию 5-дегидрошикимовой кислоты. 5-дегидрошикимовая кислота способна как прямо трансформироваться, при ее восстановлении и отщеплении молекулы воды, в 3,4-дигидроксибензойную кислоту, так и восстанавливаться до шикимовой кислоты. В свою очередь шикимовая кислота может превращаться, при ее восстановлении и аминировании, в антраниловую. В этом же пути метаболизма образуется фенилпировиноградная кислота.
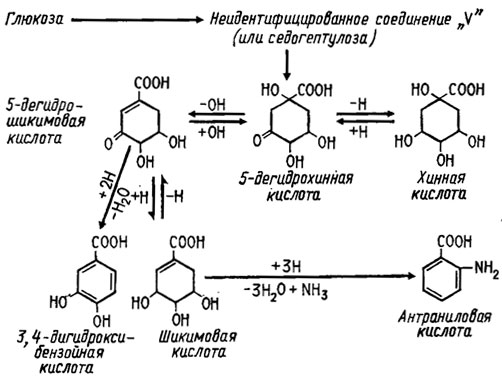
Рис. 3.14. Биосинтез ароматических соединений через шикимовую кислоту, изученный с помощью мутантов Neurospora crassa (Miller, 1961)
Второй путь биосинтеза производных фенольного ряда возможен через конденсацию соединений терпенового типа, сходных с мевалониевой кислотой, или с мономерами изопренового строения (Vanek, Sucek, 1962).
Образование ароматических соединений у грибов имеет значение не только в связи с биосинтезом антибиотиков и ряда пигментов, но также связано с их ролью в отношении формирования гумуса почвы, весьма сходного по своему составу с меланиновыми пигментами грибов. Это сходство проявляется как в элементарном составе гумуса и меланинов (Мирчинк, 1976), в среднем количестве азота между меланинами растений и животных, так и в других параметрах (экстинкция при λ = 465 нм, молекулярная масса). Меланины грибов, судя по обилию в них азота, видимо, в значительной мере составлены из остатков ароматических аминокислот подобно индольным меланинам животных, хотя, вероятно, в них есть примесь и чисто углеродсодержащих типа меланина Daldinia concentrica (Allport, Bu'Lock, 1960) или пирокатехольного меланина высших растений (Жданова, 1976).
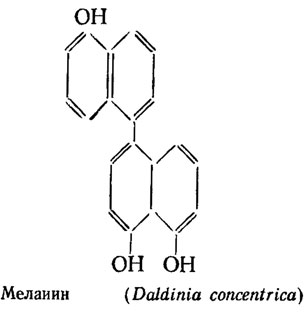
Сравнительный элементарный состав меланина показал, что он содержит приблизительно от 1 до 4% азота против 0,7% в меланине высших растений и от 5 до 9% - в меланине животных (Мирчинк, 1976; Лях, Рубан, 1972). Безазотистый меланин грибов, вероятно, синтезируется подобно стеролам в шунте терпенов, тогда как синтез индольного меланина, видимо, относится к азотному обмену и протекает по пути, изученному у животных, исходящему из шикимовой кислоты. Синтез последней описывался выше и подробно изучен на модели мутантов Neurospora crassa.
Путь биосинтеза индольного меланина исходит из тирозина и протекает с участием молекулярного кислорода и обильного у грибов фермента тирозиназы, трансформирующей тирозин сначала в диоксифенилаланин (ДОФА), затем в дофахинон и, наконец, после образования пятичленного азотсодержащего кольца, в 5,6-диоксииндол-2-карбоновую кислоту. Последняя при действии оксидазы трансформируется в красный пигмент ДОФА-хром со свойствами хинона, теряет карбоксильную группу, превращаясь в 5,6-диоксииндол, и окисляется затем в соответствующий хиной, способный в дальнейшем при окислении полимеризоваться, образуя меланин.
Пути образования меланина у паразита хлопчатника Verticillium dahliae (Bell et ah, 1976; Sete, Yonohara, 1977; Stipanovic, Bell, 1977), у паразита риса Piricularia oryzae (Sisler, Tokousbalides, 1979) обобщены Сислером. Этот путь биосинтеза меланина исходит из ряда гидроксилированных и окисленных нафталинов, как сциталон и вермелон, из которых далее формируется 1,8-дигидроксинафталин, конденсирующийся в меланин. Угнетение трициклазолом образования меланина у P. oryzae не сопровождается подавлением синтеза сходного с его предшественниками токсина P. oryzae - пирикуляриола, а, наоборот, усиливает его продукцию, что указывает на конкуренцию его биосинтеза с биосинтезом меланина.
Грибы способны образовывать и другие конденсированные соединения, например, имеющие характерное пятичленное лактонное кольцо тетроновой кислоты (Bu'Lock, 1961). Эти соединения образуются путем конденсации какой-либо оксикислоты, чаще молочной или яблочной, с другой кислотой, например уксусной:
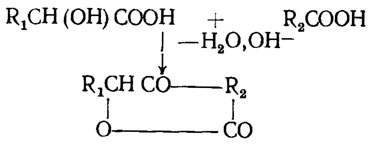
Особенно часто этот тип соединений встречается у видов рода Penicillium (P. charlesii, P. viridicatum, P. terrestre, P. cinerascens), хотя они есть и у других грибов (табл. 3.8).
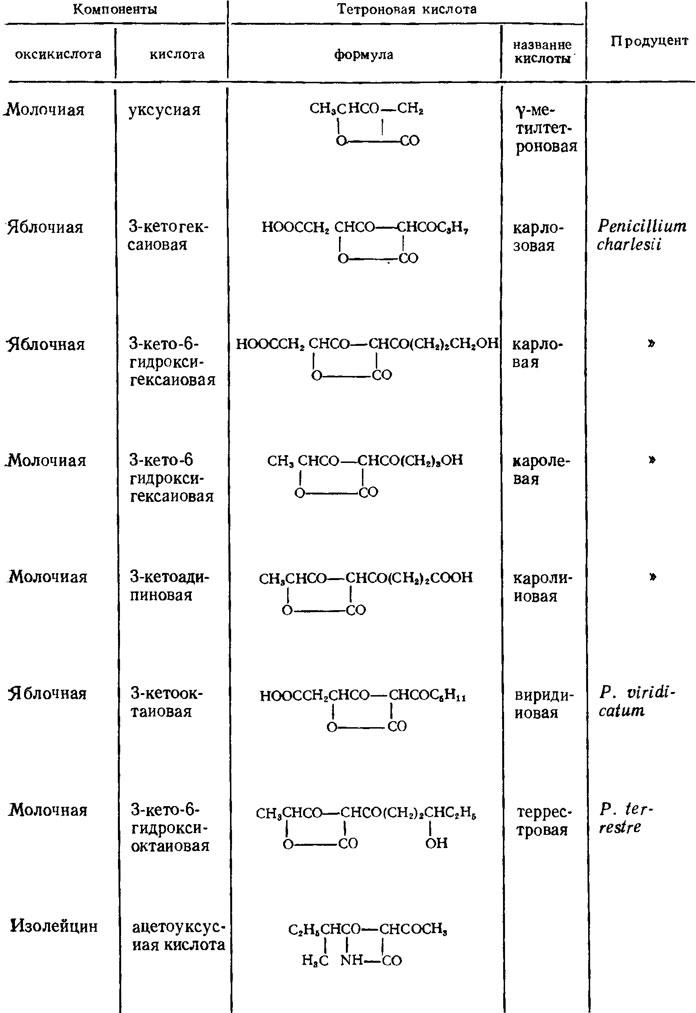
Таблица 3.8. Тетроновые кислоты плесневых грибов (Bu'Lock, 1961)
В числе образуемых грибами органических кислот встречаются и такие, которые синтезируются путем дополнительных трансформаций кислот цикла Кребса. К таким относится образуемая Aspergillus terreus и A. itaconicus итаконовая кислота, видимо, получающаяся в результате метилирования по второму углероду и окисления янтарной кислоты:
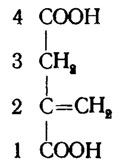
Она имеет большое практическое значение как сырье для изготовления синтетических полимеров. Очень часто встречаются у грибов также гетероциклические соединения с включением в углеродный скелет какого-либо другого атома, чаще всего азота или серы, или с перемежающейся конденсацией аминокислот с жирными кислотами, например, при синтезе антибиотиков рода Fusarium, носящих название депсипептидов.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'