
Аминокислоты, пептиды и белки
С точки зрения химика, пептиды организованы довольно сложным образом. Их молекулы представляют собой полимеры, то есть цепочки из нескольких мономерных единиц, называемых аминокислотами. В свою очередь, молекулы аминокислот устроены так, что на одном их конце находится группа NH2, или аминогруппа, а на другом - группа СООН, придающая этому химическому соединению свойства кислоты. Отсюда и возникает название: аминокислота. Отсюда же следуют и общеупотребительные в пептидном деле обозначения, концов молекулы: N- и С-конец.
Между описанными двумя концевыми группами могут быть в принципе расположены любые комбинации атомов, и все равно полученные из них молекулы будут иметь полное право считаться аминокислотами. Но пептиды, функционирующие в организме, построены, как правило, лишь из вполне определенных аминокислот вида;
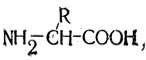
причем когда аминокислоты соединяются в цепочку (с выделением молекул воды), то типичный пептид может быть представлен как:
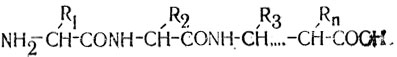
Элемент - CONH -, называемый пептидной группой, или пептидной связью, повторяясь, образует остов молекулы (в дословном переводе с английского backbone - костяк, скелет), а различные типы атомных группировок, ответвляющиеся от остова и условно обозначенные буквами R1, R2, R3.., Rn, называются боковыми цепями.
Таким образом, остов молекулы пептида является монотонным повторением одного и того же сочетания атомов (кристаллографы, к вящей зависти представителей других естественных наук, выразились бы куда более изящно, употребив легализованное ими выражение "монотонный атомный мотив"). Зато каждая боковая цепь имеет свою яркую индивидуальность. В целом это все напоминает модные в свое время ожерелья из разноцветных и разнокалиберных кусочков пластмассы - тем более что молекула пептида иногда бывает замкнута в кольцо.
Или еще более близкое сравнение: представьте себе вереницу взявшихся за руки артисток кордебалета в самых разнообразных одеяниях, исполняющих на сцене сложный танец так, что цепочка остается ненарушенной. Надо признаться, что этот пример не вполне оригинален: однажды в солидном научном учреждении снимался популярный телефильм о пептидах, и одаренный буйной фантазией сценарист предложил изобразить молекулу пептида на цветном телеэкране именно в таком виде.
Увы, консервативные ученые консультанты наотрез отказались иллюстрировать свои научные достижения с помощью легкомысленного кордебалета, что, по-видимому, и повлекло за собой неизбежный провал фильма. Конечно, теперь эти консультанты горько сожалеют о своей несгибаемой принципиальности, не позволившей им дать полное представление о пептидах если не миллионам телезрителей, то хотя бы некоторым из балерин, но - уже поздно.
Разнообразие аминокислот, из которых образуются природные пептиды, не так уж велико: подавляющее большинство пептидов состоит из двадцати типов мономеров, различающихся, как уже было сказано, характером боковых цепей. При включении в молекулу пептида каждая аминокислота превращается в так называемый аминокислотный остаток, которых, естественно, будет тоже двадцать:


Здесь приведены, наряду с названиями, два способа обозначений аминокислотных остатков: трехбуквенный и однобуквенный; в научной литературе приняты оба, хотя некоторое предпочтение отдается первому.
Итак, для несостоявшегося пептидного балета понадобилось бы всего двадцать типов танцовщиц или, за неимением такого разнообразия хореографических индивидуальностей, хотя бы двадцать типов балетных костюмов. Можно сказать и по-другому, более информативно и более вычурно: алфавит одного из языков, на которых организм отдает приказы самому себе, насчитывает двадцать букв - тех самых, что стоят в третьей колонке только что записанной таблицы. А задача исследователя как раз и состоит в овладении этим языком. В худшем случае хотелось бы понимать, какой смысл несут его "слова" (например, DRVYIHPF или TKPR), мелькающие на страницах научных журналов, а в лучшем - самому "заговорить" на этом языке, создавая осмысленные "буквосочетания" из аминокислот.
Однако об изучении "пептидного языка" речь еще будет идти впоследствии, и очень подробно. А пока вернемся к аминокислотам, упомянутым в таблице. В свое время они пользовались звучным титулом "магического набора", поскольку те, кто начинал систематические исследования пептидов, были немало поражены обстоятельством, на которое вряд ли обратил внимание кто-нибудь из читателей: а почему именно эти двадцать аминокислотных остатков попали в состав природных пептидных молекул?
Ответ на поставленный вопрос внешне довольно прост: инструкция по включению в пептидную цепь именно этих двадцати аминокислот накрепко записана в организме на "нуклеиновом языке" в молекулах нуклеиновых кислот, размножение которых и обеспечивает передачу всей генетической информации об организме от поколения к поколению. Эти "самые главные молекулы" (по удачному выражению профессора М. Франк-Каменецкого) представляют собой очень длинные цепочки, построенные из четырех типов мономеров, называемых нуклеотидами (поэтому алфавит "нуклеинового языка" в отличие от "пептидного" состоит всего из четырех "букв"). При этом каждое из шестидесяти одного возможного сочетания из трех нуклеотидов (три сочетания исключаются) прочитывается организмом как приказ выбрать из своих "запасов" какую-либо аминокислоту.
Соответствие между тройками нуклеотидов и выбираемыми аминокислотами устанавливает генетический код, открытие которого до сих пор можно смело считать самым большим достижением биологии XX века. А правилами этого кода предусмотрен выбор только описанных выше двадцати аминокислот.
Правда, в природных пептидах, хоть и редко, встречаются другие аминокислотные остатки, например, пироглутамат или оксипролин, но они, как говорят на молекулярно-биологическом жаргоне, не кодируются, а получаются в организме с помощью разных биохимических ухищрений из аминокислот все того же "магического набора", уже включенных в состав пептидных молекул.
Надо признаться, что описание в рамках всего трех абзацев сложнейшей проблемы, официально называемой ни много ни мало "центральной догмой молекулярной биологии", может несколько дезориентировать читателя. Ведь невольно создается впечатление, что решение проблемы - "почему именно эти двадцать аминокислот" - далось легко и просто. На самом же деле это потребовало многих лет труда, сотен, если не тысяч изощренных экспериментов и немалых чисто человеческих разочарований, ибо об "устройстве", например, генетического кода были выдвинуты десятки остроумнейших гипотез, а уцелела в результате лишь одна, предложенная английским ученым Ф. Криком и американцами М. Ниренбергом и С. Очоа.
Мало того, превращение этой гипотезы в общепризнанную (на уровне Нобелевской премии) теорию немедленно выдвинуло новую проблему: почему данная тройка нуклеотидов означает выбор именно данной аминокислоты? И вот уже на этот вопрос на сегодняшний день полного ответа не знает никто, и поэтому ученые вынуждены ставить новые эксперименты, придумывать новые гипотезы, и так далее. Иными словами, в науке удачный ответ -* это только повод для новых вопросов, и в этом смысле воспеваемая восторженными журналистами творческая жизнь научных работников отличается от бега белки в колесе лишь возможностью в случае успеха расширить размеры колеса.
Впрочем, забудем эту печальную (но зато правдивую) сентенцию и с новыми силами возвратимся к изложению: ведь мы теперь твердо знаем, что пептиды - это цепочки аминокислот "магического набора", выстроенные в ряд (его еще называют "аминокислотная последовательность") от N- до С-конца. Более того, оказывается, что, зная, как построены пептиды, мы тем самым знаем и то, как построены белки, вещества, выполняющие в организме множество чрезвычайно важных функций - от обеспечения правильного течения биохимических реакций [белки-ферменты) до использования в качестве строительного материала (вспомним любимый журнал "Здоровье": белки, жиры, углеводы...).
По представлениям того же химика белки - это точно такие же цепочки из тех же двадцати типов аминокислотных остатков, выстроенные в такую же последовательность от N- к С-концу, но включающие в нее гораздо больше мономеров, чем пептиды. Так что для химика более привычным, чем формула журнала "Здоровье", является словосочетание "белки и пептиды", поскольку химия пептидов и химия белков не слишком далеки друг от друга. Даже регулярно созываемый Всесоюзный симпозиум носит название "по химии белков и пептидов". Поэтому химику трудно провести четкую грань между белком и пептидом; обычно считается, что цепочка размерами где-то не более 50 аминокислот - это еще пептид, а сверх того - уже белок.
В нашей книге речь пойдет вообще только об олигопептидах, состоящих не более чем из десяти-пятнадцати аминокислот (по-гречески "олигос" означает "малый"). Конечно, разделение это условное, и вообще вряд ли можно его обосновать с чисто химической точки зрения: количество аминокислотных остатков в цепи переходит в новое качество скорее в отношении физических свойств молекулярной цепочки. Но и с точки зрения биолога, связь между белками и пептидами в организме оказывается весьма тесной, и чтобы убедиться в этом, достаточно прочитать следующий раздел.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'