
Молекулярная топохимия
Роль первооткрывателей, первопроходцев и вообще "тех, кто был первым" - неважно, в какой из областей человеческой деятельности, - настолько широко, подробно и, главное, квалифицированно описана в художественной литературе, что, говоря об особенностях, с которыми связано освоение передовых рубежей в науке, можно ограничиться лишь одним замечанием.
В науке очень важно, конечно, подметить ту или иную взаимосвязь явлений; еще важнее - выдвинуть идею о возможном обосновании такой взаимосвязи; и еще важнее - подтвердить новую идею на эксперименте; но самое главное, важное и трудное: убедить других (и себя) в необходимости изменения всего предшествующего подхода к проблеме и построить на основании новой идеи вполне конкретную и поддающуюся проверке теорию, разработанную до мелочей. Ибо всякого рода "гениальные догадки" - это прекрасно, но все же автором теории атомного строения материи история науки считает скорее английского естествоиспытателя Дж. Дальтона, чем философов Левкиппа и Демокрита.
Возвращаясь к нашей тематике, стоит в этой связи отметить, что сам по себе факт зависимости биологических функций пептидных молекул от их конформаций был ясен ведущим специалистам уже в начале 60-х годов; в связи с этим стоит упомянуть имена чешского ученого Й. Рудингера, швейцарского химика Р. Швицера и американца Р. Вальтера. Однако ранние попытки установить, в чем именно выражается связь "конформация - функция", носили разрозненный характер, и результаты исследований не удавалось обобщить в более или менее стройную систему взглядов.
Первая подобная система появилась лишь через несколько лет и получила. распространение и признание под названием "топохимический подход": его авторами были советские ученые Ю. Овчинников (ныне академик и вице-президент АН СССР) и В. Иванов (ныне член-корреспондент АН СССР).
Ю. Овчинников и В. Иванов изучали циклические депсипептидные антибиотики - соединения, остов которых замкнут в кольцо (как змея Галена, кусающая свой собственный хвост) и состоит из чередующихся один за другим двух типов модификаций пептидной группы CONH; СОN(СН3) и COO - по валентному строению обе получающиеся атомные группировки сходны с пептидной.
Кроме того, эти антибиотики являлись как раз тем редким случаем, когда в природных соединениях появляются "правые" боковые цепи: "правые" и "левые" их варианты также чередовались один за другим вдоль по остову. По такому принципу построен, в частности, природный шестичленный антибиотик, называемый энниатином В, в котором все боковые цепи имеют одну и ту же химическую природу, но представляют собой энантиомеры друг друга.
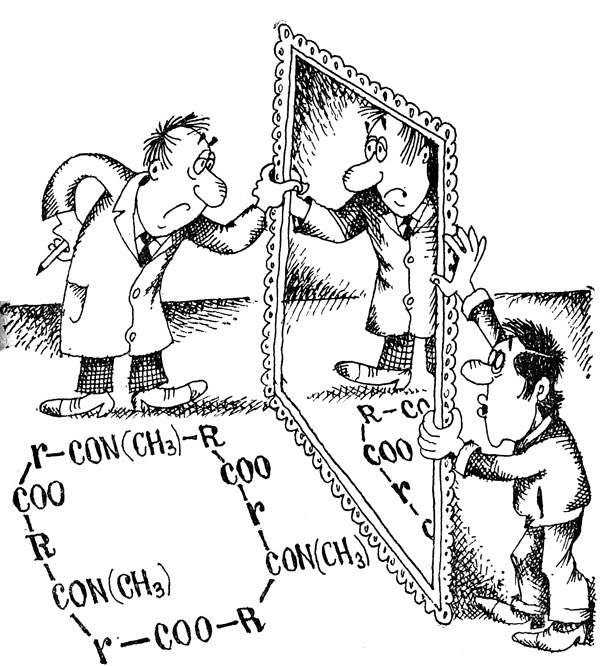
Энниатином
Исследователи задались вопросом: что будет, если химическим путем воспроизвести энантиомер (то есть заменить все "правые" боковые цепи на "левые" и наоборот) полной молекулы энниатина В? Схематически такую пару молекул можно было бы изобразить следующим образом:
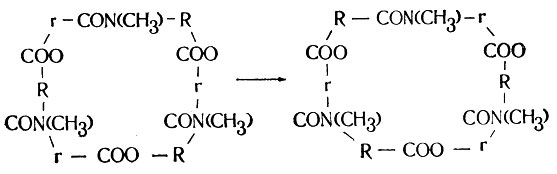
Здесь буквы г и R обозначают "правые" и "левые" боковые цепи, а примыкающие к ним атомы Н опущены. Молекулярные "кольца" на разных сторонах схемы кажутся различными, особенно в связи с тем утверждением, что способ пространственной ориентации боковой цепи - "правый" или "левый" - имеет огромное значение для функциональной активности молекулы. Однако если повернуть второе кольцо вокруг центральной оси на 60 градусов, строчные и прописные буквы R будут чередоваться точь-в-точь так, как в первом кольце: разница между кольцами сведется лишь к заменам всех модификаций остова типа СОО на модификации CON (СН3) и наоборот.
Но ведь обе эти модификации сходны между собой и с пептидной группой; поэтому есть основания полагать, что, какой бы ни была конформация исходной молекулы энниатина В, конформация его энантиомера будет примерно такой же, а стало быть, и активность аналога сохранится. Это предположение Ю. Овчинникова и В. Иванова полностью подтвердилось в эксперименте, что уже само по себе означало поистине блестящий результат: ведь впервые было зафиксировано явление полной функциональной эквивалентности асимметрического природного соединения и его зеркального антипода-энантиомера.
История с энниатином В послужила, однако, лишь исходным рубежом развития общего топохимического подхода, основную задачу которого можно было бы сформулировать примерно так: найти способ создания аналогов пептидных молекул с сохранением их конформации, понимаемой как взаимное пространственное расположение боковых цепей. И вновь анализ задачи начался с циклических пептидов, но на этот раз рассматривался самый общий случай, например, произвольный циклотет-рапептид I и его энантиомер II:
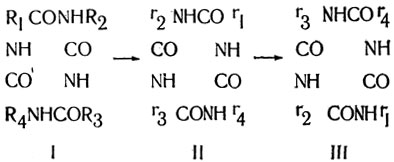
Энантиомер II получается из исходного соединения I зеркальным отражением в плоскости, перпендикулярной госкости страницы, - так же, кстати говоря, как и на юдыдущей схеме превращения энниатина В. При этом "левые" боковые цепи R переходят в "правые" г, но, поскольку все они различны, никакими вращениями вокруг центральной оси совместить молекулы I и II невозможно (хотя при таком отражении боковые цепи R и г одинаковым номером направлены в одну и ту же сторону). Но если изменить порядок включения боковых: цепей в остов соединения II на обратный, синтезировав так называемый ретроаналог, получится соединение III, которое совмещается с начальным соединением I поворотом на 180 градусов вокруг центральной оси; однако вместо обычной пептидной группы CONH в остове соединения III будет фигурировать ретроэлемент - группа NHCO.
Если же этим различием пренебречь, то можно постулировать в качестве общего принципа сходство конформаций циклического пептида и соответствующего ему ретро-энантио-аналога, то есть соединения, где порядок включения аминокислот в пептидную цепь заменен на обратный, а сами аминокислоты замещены их энантиомерами. Подобное утверждение было проверено на примере одного из аналогов пептидного антибиотика грамицидина S и в очередной раз оказалось вполне справедливым.
Поскольку рассуждения, приводимые выше, приложимы, вообще говоря, к любым пептидам, а не только к циклическим, авторы "топохимического подхода" распространили его и на линейные пептиды. Здесь, однако, пришлось принять во внимание, что гипотетический линейный пептид:
NH2-R1-CONH-R2-CONH-R3-COOH
и его ретро-энантио-аналог:
HOOC-r1-NHCO-r2-NHCO-r3-NH2,
помимо инверсии CONH → NHCO, различаются еще и расположением очень важных функционально и активных химически концевых групп NH2 и СООН. Впрочем, если заблокировать концы молекул химически нейтральными атомными группировками (а в арсенале пептидной химии они представлены в достаточном ассортименте), "топохимический подход" может оказаться применимым и в этом случае. Действительно, пользуясь изложенным принципом, нашли, например, новые пептидные соединения - ретро-энантио-аналоги, успешно конкурирующие со своими "прародителями" при взаимодействии с ферментами-пептидазами.
Таким образом, Ю. Овчинников и В. Иванов явились одними из пионеров конформационно-функциональных исследований пептидов, значительно опередив в этом отношении многих советских и зарубежных исследователей: достаточно напомнить, что в годы создания "топохимического подхода" представление о конформациях пептидов было почти что чисто умозрительным, поскольку и экспериментальные и теоретические методы изучения этих конформаций тогда еще только становились на ноги. Поэтому и большинство гипотез о факторах, определяющих биологическую активность пептидов, по существу, не выходило за пределы "линейных" соображений, как, например, изложенная в предыдущей главе "теория сигнатур".
"Топохимический подход" к исследованию взаимосвязи пространственных структур циклических пептидов и их функций в организме стал впоследствии мощным инструментом, с помощью которого Ю. Овчинников и В. Иванов вскрыли целый ряд закономерностей в молекулярных механизмах весьма важного биологического явления: переноса ионов, сквозь клеточные мембраны; в результате этой многолетней работы обоим ученым была присуждена Ленинская премия 1978 года. Да и другие исследователи неоднократно и небезуспешно руководствовались при направленном поиске эффективных пептидных аналогов "топохимичеоким подходом".
И тем не менее "топохимический подход" знаменовал собой лишь начало грядущей эры молекулярной топологии, достигшей расцвета в наши дни, когда пространственные формы пептидов научились исследовать настолько подробно, что заметными стали даже следствия атомной перегруппировки GONH в NHCO, не принимавшиеся ранее в расчет как незначительные. Сейчас "линейное" мышление в пептидном драг-дизайне выглядит уже анахронизмом; но чтобы мыслить в "трехмерных" категориях, необходимо не только усваивать и понимать информацию о пространственном строении пептидных молекул, предоставляемую весьма изощренными методами исследования, но и четко оценивать степень ее достоверности. Именно на методах изучения конформаций пептидов и их результатах мы и остановимся в дальнейшем.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'