
Антибиотики
Среди химиотерапевтических средств видное место занимают антибиотики, представляющие собой группу новых высокоэффективных лечебных препаратов, которые вошли в медицинскую практику за последние 15 лет. За этот короткий срок антибиотики заняли ведущее место в арсенале медикаментозных средств, применяемых в целях терапии инфекционных заболеваний.
Уже давно было сделано наблюдение, что в природе существуют микроорганизмы, отличительным свойством которых является способность подавлять развитие других микроорганизмов в окружающей среде. Явление, характеризующееся тем, что в присутствии одного микроба размножение другого становится невозможным, получило название антибиоза (anti — против, bios — жизнь). Выделяемые микробами вещества, подавляющие жизнедеятельность других микроорганизмов в среде, получили название антибиотических веществ, или антибиотиков. Термин «антибиотики» в на" стоящее время общепризнан и получил широкое распространение. Всестороннее изучение антибиотиков как лечебных препаратов представляет собой одну из важнейших проблем современной медицины.
Л. Пастер впервые открыл явление антагонизма микробов. Его ученик — русский микробиолог И. И. Мечников — показал, что при введении в кишечник молочнокислых бактерий погибают многие болезнетворные бактерии, ранее заселявшие кишечник. И. И. Мечниковым были сформулированы основные положения учения об антибиозе.
В настоящее время описано большое количество антибиотиков (исчисляемое сотнями). Отличительными свойствами всех антибиотиков является избирательное действие на микробы. Антибиотики, вырабатываемые живой клеткой, не относятся к общеклеточным ядам, подобно сулеме и фенолу, которые оказывают губительное действие на все виды клеток. Каждый антибиотик эффективен в отношении определенной группы микробов: одни из них он подавляет резко, другие — слабо, а в отношении некоторых не действует совсем. На образующую его микробную клетку антибиотик тормозящего влияния не оказывает. Каждый антибиотик обладает определенным антимикробным спектром действия, определяющим его значение для целей практической медицины.
Источником получения антибиотиков служат различные микроорганизмы. Некоторые авторы антибиотиками называют также и продукты, получаемые из животных и растительных тканей, обладающие антимикробным действием. Однако такое расширение понятия об антибиотиках вносит много путаницы и не может быть признано правильным. Следует упомянуть, что антимикробные вещества, содержащиеся в растениях, носят специальное название «фитонциды».
Большое значение при оценке нового антибиотика имеет его поведение в присутствии белка. Многие антибиотики при контакте с белковыми веществами теряют свою активность и поэтому не используются в качестве лечебных средств, так как в организме они будут инактивироваться, образуя с белками комплексы, не оказывающие антибактериального действия. Другие антибиотики, обладая мощным антибактериальным действием, не находят применения в медицинской практике из-за высокой токсичности для животных и человека. В связи с указанным только немногие из большого числа открытых антибиотиков используются в качестве лечебных препаратов. Среди них большое значение имеют пенициллин, стрептомицин (см. Средства для лечения туберкулеза и проказы), хлорамфеникол, биомицин, террамицин, тетрациклин, альбомицин, эритромицин и некоторые другие.
Пенициллин
Пенициллин представляет собой продукт жизнедеятельности некоторых видов плесневых грибков (Penicillium notatum, Penicillium chryso-genum и др.).
Антибактериальные свойства пеницилла, или зеленой плесени, впервые были установлены русскими учеными Манассеиным в 1871 г. и Полотебновым в 1872 г. Они применяли зеленую плесень для лечения гнойных ран и хронических язв (различной этиологии) и получали терапевтический эффект. Позднее, в 1904 г., русский ученый Тартаковский сделал наблюдение, что зеленая плесень оказывает угнетающее действие на возбудителя эксудативного тифа кур.
Флеминг (1928) сделал случайное наблюдение, что колонии зеленой плесени подавляют рост золотистого стафилококка, и показал, что это явление зависит от выделения плесенью в окружающую среду особого вещества, которое он назвал пенициллином. Позднее были разработаны способы промышленного получения и очистки пенициллина, установлена его химическая формула и осуществлен синтез химическим путем. Оказалось, что существует несколько видов пенициллина, имеющих сходное строение и отличающихся лишь радикалом в боковой цепи. Общая формула строения пенициллина следующая:
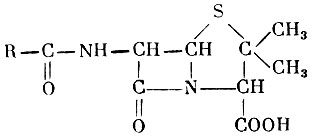
Пенициллин
В зависимости от характера радикала (R) различают много отдельных видов пенициллина (табл. 5).

Таблица 5
Наибольшее значение для медицинской практики имеют бензилпенициллин (пенициллин G) и феноксиметилпенициллин (пенициллин V).
В промышленном масштабе оба антибиотика получаются путем ферментации. Пенициллин О интересен тем, что не вызывает аллергических реакций у больных с повышенной чувствительностью к пенициллину G.
В медицинской практике используются соли пенициллина, чаще всего натриевая или калиевая.
Пенициллин оказывает выраженное антимикробное действие на многие виды бактерий: стафилококк, стрептококк, пневмококк, менингококк, возбудители столбняка, газовой гангрены, сибирской язвы и сифилиса. Не чувствительны к пенициллину кишечная группа бактерий, возбудители чумы и туляремии, риккетсии, вирусы и простейшие. Сила действия пенициллина на микробы очень велика: 1/50000000 г препарата вызывает гибель 200 000 000 бактерий.
Механизм антимикробного действия пенициллина в настоящее время изучен еще не полностью. Имеются предположения, что в присутствии пенициллина микробы теряют способность ассимилировать необходимые для размножения аминокислоты из окружающей среды и синтезировать необходимые им белковые вещества. Микробная клетка теряет способность к делению, в результате чего образуются крупные формы бактерий. Бактерицидное действие пенициллина обнаруживается в том случае, если пенициллин добавляется к активно размножающейся культуре. В противоположном случае, т. е. при отсутствии процесса размножения (сохранение культуры при низкой температуре, отсутствие питательных веществ) пенициллин гибели микробов не вызывает.
Многочисленные исследования показывают, что при выращивании чувствительных к пенициллину микробов в присутствии таких доз пенициллина, которые сами по себе недостаточны для гибели микробов (сублетальные концентрации), образуются новые формы микроорганизмов, которые в десятки и сотни раз более устойчивы к пенициллину, чем исходные. Показано, что лекарственная устойчивость микроорганизмов не является результатом того, что они обладают способностью разрушать пенициллин. Пенинциллиноустойчивые расы, по-видимому, отличаются от исходных рас своим обменом веществ.
Бензилпенициллин — нестойкое вещество. Различные влияния вызывают его разрушение. Он гигроскопичен, поглощение же влаги приводит к его инактивации. Так же быстро бензилпенициллин разрушается в растворах. Этот процесс усиливается с повышением температуры окружающей среды. Бензилпенициллин разрушается при длительном солнечном освещении, в присутствии кислот и щелочей, окислителей, солей тяжелых металлов, алкоголя. Феноксиметилпенициллин отличается значительно большей устойчивостью по сравнению с бензилпенициллином, в частности к кислотам. Разрушают пенициллин и ферменты многих бактерий (пенициллиназа). Поэтому всякие манипуляции с пенициллином (приготовление растворов и других лекарственных форм) должны производиться в стерильных условиях, чтобы предохранить его от разрушения микробной флорой. Необходимо иметь в виду, что микробы, способные инактиви-ровать пенициллин, в большом количестве содержатся в воздухе.
Пенициллин, обладая хорошей растворимостью в воде и низким молекулярным весом, легко проникает через стенку капилляров в ткани организма. Исключение составляет центральная нервная система и спинномозговая жидкость. В них обнаруживаются низкие концентрации пенициллина по сравнению с его уровнем в крови. Пенициллин слабо проникает в брюшную и плевральную полости. Мало его содержится и в тканях глаза при парентеральном введении.
Из желудочно-кишечного тракта всасывание бензилпенициллина происходит очень неравномерно, причем около 80% введенного количества разрушается пищеварительными соками. Вследствие этого бензилпенициллин приходится вводить внутрь в очень больших дозах. Феноксиметилпенициллин отличается от других пенициллинов устойчивостью в кислой среде. При введении внутрь он хорошо всасывается и в крови создается высокая концентрация пенициллина, удерживающаяся в течение 3—4 часов. После внутривенной инъекции около 75% введенного бензилпенициллина через 15—30 минут покидает кровяное русло, в последующие 3—4 часа в крови определяются низкие концентрации пенициллина, недостаточные для проявления бактериостатического эффекта. Более рациональным является внутримышечный способ введения бензилпенициллина, так как максимальная концентрация в крови в этом случае определяется через 15 минут, через 60—90 минут она уменьшается примерно вдвое и лишь к третьему часу после введения содержание пенициллина падает до низких цифр. Поэтому наиболее целесообразно вводить пенициллин внутримышечно повторно в течение суток через каждые 3—4 часа. Так как частые инъекции тягостны для больного и затрудняют проведение лечения пенициллином в амбулаторных условиях, было предложено много способов, направленных на то, чтобы удлинить циркуляцию пенициллина в организме.
После того как было установлено, что около 40—50% введенного парентерально пенициллина выделяется почками в активной форме, были сделаны попытки блокировать выведение пенициллина почками с помощью препаратов, угнетающих функцию почек (диодраст, каронамид). Но предложенный метод не нашел широкого распространения, так как блокада почек не является безразличной для больного. Другие способы были направлены на то, чтобы затруднить всасывание пенициллина из той области, куда была произведена инъекция, т. е. создать депо на месте введения пенициллина, откуда он постелено будет поступать в общий ток крови. В настоящее время широко используется метод введения пенициллина в растворах новокаина. Образующаяся при этом новокаиновая соль пенициллина, будучи плохо растворимой в воде, после инъекции медленно всасывается в кровь. В связи с этим больной освобождается от многократных инъекций пенициллина. Комбинированное применение пенициллина с новокаином позволяет ограничиваться 2—3 инъекциями в сутки, причем в крови удерживается концентрация пенициллина, достаточная для проявления терапевтического эффекта. На основе этого принципа создан препарат пенициллина — новоциллин. С целью создать высокую концентрацию пенициллина в очаге инфекции его вводят непосредственно в область локализации инфекционного процесса. Заслуживает внимания метод введения антибиотиков в аэрозолях. При таком пути введения раствор или порошок антибиотика распыляется с помощью специальных распылителей. Величина частиц колеблется от 2 до 5 м. В мелкораздробленном состоянии антибиотик вдыхается. Попадая в дыхательные пути больного, он оказывает не только местное, но и резорбтивное действие, так как происходит всасывание препарата в кровь.
Роль макроорганизма в успехе пенициллинотерапии, как и всякой химиотерапии, чрезвычайно велика. При пониженной сопротивляемости организма применение пенициллина даже в больших дозах иногда не оказывает терапевтического действия, поэтому лечение пенициллином должно проводиться в комплексе с другими терапевтическими воздействиями, направленными на усиление защитных свойств организма. Так, для усиления процессов иммуногенеза рекомендуется сочетанное применение антибиотиков с вакцинотерапией. Лечение пенициллином, как и другими антибиотиками, должно проводиться при соблюдении определенных условий. Для эффективности лечения важным условием является чувствительность возбудителя заболевания к данному антибиотику.
Биологическая активность пенициллина выражается в единицах действия (ЕД). За единицу действия принимают активность 1 единицы пенициллина (0,6 мг натриевой соли чистого кристаллического бензил-пенициллина). Таким образом, 1 мг препарата обладает активностью, равной 1666 ЕД.
Дозы пенициллина, применяемые у больных, варьируют в значительной степени. Они зависят от тяжести инфекции, ее характера и общего состояния организма. Лечение необходимо проводить достаточно большими дозами пенициллина и достаточно длительное время. Разовая доза пенициллина составляет 100 000 — 200 000 ЕД и более. Длительность лечения варьирует от нескольких дней до нескольких месяцев в зависимости от характера заболевания.
Многие клиницисты отмечают, что под влиянием пенициллина изменяется клиническая картина заболевания. Иногда она становится настолько неясной, что диагностика затрудняется, так как уменьшаются боли, улучшается самочувствие больного, маскируя тяжесть заболевания, в то время как местные симптомы болезни обостряются. Из-за внешнего благополучия при хирургических заболеваниях упускается время для неотложного оперативного вмешательства. Поэтому лечение пенициллином без надлежащего врачебного контроля проводить не рекомендуется.
Несмотря на малую токсичность пенициллина, при его применении, особенно повторном, все же наблюдаются побочные явления. За последнее время накопилось много фактов, свидетельствующих о том, что у некоторых больных обнаруживается высокая чувствительность к этому антибиотику. Побочные реакции особенно часто встречаются при повторном длительном лечении пенициллином. Они выражаются различного рода сыпями (эритема, крапивница и т. п.). У медицинского персонала иногда возникают контактные дерматиты, сопровождающиеся отторжением эпителия. Наблюдаются также явления, напоминающие сывороточную болезнь (зуд, крапивница, боли в суставах, повышение температуры), агранулоцитоз. Описаны даже смертельные исходы, наступившие непосредственно вслед за инъекцией пенициллина в результате анафилактического шока. Назначая пенициллин, необходимо тщательно опросить больного и выяснить, не имели ли место в прошлом явления повышенной чувствительности к лекарственным препаратам, в том числе к пенициллину. Обращается особое внимание на наличие припухлости и зуда на месте инъекции, неприятного вкуса во рту при сосании таблеток, растройства со стороны желудочно-кишечного тракта, затруднения дыхания и обмороков. Применение антигистаминных препаратов снижает частоту побочных явлений и их интенсивность. При анафилактическом шоке внутривенно капельным методом вводят адренокортикотропный гормон (АКТГ).
Применение пенициллина может иногда сопровождаться развитием грибковых заболеваний. Обычно развитию патогенных грибков на слизистых оболочках препятствует нормальная бактериальная флора, которая там обитает. Подавление бактериальной флоры пенициллином может повести к размножению грибков, на которые этот антибиотик не действует. Чаще всего наблюдается развитие дрож-жеподобного грибка Candida albicans. Особенно опасным является возникновение генерализованного кандидоза, с которым трудно бороться.
Серьезным осложнением в процессе лечения антибиотиками являются энтериты (поражениятонкого кишечника). Они вызываются резистентными к антибиотику формами бактерий (кишечной палочкой, стафилококками, энтерококками). Энтериты проявляются холероподобным поносом и усилением порозности кишечной стенки. Последнее обстоятельство способствует проникновению из кишечника в кровь болезнетворных микробов. В некоторых случаях энтериты заканчиваются летально.
Пенициллин, по-видимому, повышает свертываемость крови, что может привести к возникновению опасного для жизни тромбоэмболического состояния (инфаркт). В связи с этим у лиц с уже повышенной до лечения свертываемостью крови пенициллин следует назначать с осторожностью.
Препараты
Натриевая соль пенициллина, ФVIII. Аморфный желтый порошок или сухая пористая масса желтого или оранжевого цвета, хорошо растворимая в воде. Выпускается в специальных флаконах в стерильном виде. Применяется для изготовления инъекционных и других растворов, а также для мазей и других лекарственных форм.
Натриевая соль бензилпенициллнна кристаллическая, ФVIII. Белый порошок или сухая пористая масса белого или желтовато-розового цвета, хорошо растворимая в воде. Используется для приготовления растворов, для инъекций и ингаляций, в частности для внутривенных и спинномозговых инъекций. Выпускается в специальных флаконах в стерильном виде.
Калиевая соль бензилпенициллина кристаллическая. Белый порошок, хорошо растворимый в воде. Применяется для изготовления растворов. Этот препарат не рекомендуется применять для внутривенных и спинномозговых инъекций. Выпускается в стерильных герметически закрытых флаконах.
Новоциллин (Novocillinum). Суспензия новокаиновой соли бензил-пенициллина в персиковом масле. Применяется для внутримышечных инъекций в качестве препарата пенициллина с длительным действием (обеспечивает действие до 48 часов). Выпускается в специальных флаконах в стерильном виде.
Новокаиновая соль пенициллина. Белый порошок, плохо растворимый в воде. Выпускается в специальных флаконах в стерильном виде. Предназначена для внутримышечных инъекций в виде взвеси в воде, физиологическом растворе или водном растворе протаминсульфата (экмолина) в качестве препарата пенициллина с длительным действием (в течение 24—36 часов).
Бициллин (Bicillinum). Соль бензилпенициллина с дибензилэтилендиамином. Белый тонкий порошок, очень плохо растворимый в воде. Выпускается в специальных флаконах в стерильном виде как таковой или в смеси с бензилпенициллином. Предназначен для внутримышечных инъекций в качестве препарата с весьма длительным действием. В зависимости от дозы препарата действие его может продолжаться от 1 до 4 недель и более. Иногда на курс лечения бывает достаточно одной инъекции препарата. При необходимости обеспечить быстрое наступление действия бициллин применяют в смеси с бензилпенициллином.
Феноксиметилпенициллин (Penicillin V). Белый порошок, плохо растворимый в воде, устойчивый к действию кислот. Выпускается в таблетках для приема внутрь.
Левомицетин и синтомицин
Большую группу составляют антибиотики, продуцентом которых являются актиномицеты. К ним относятся стрептомицин, левомицетин, биомицин, террамицин, тетрациклин, альбомицин и многие другие. Актиномицеты, или лучистые грибки, широко распространены в природе. Особенно много их в почве, причем в самых разнообразных районах земного шара. Актиномицеты легко приспосабливаются к окружающей среде и развиваются там, где другие микроорганизмы погибают. Установлено, что актиномицеты выделяют в окружающую среду антибиотические вещества, отличающиеся качественным разнообразием (антибактериальным спектром) в отношении влияния на бактерии. Ввиду широкого распространения лучистых грибков в природе и их способности выделять отличающиеся друг от друга антибиотические вещества поиски новых антибиотиков именно среди актиномицетов являются многообещающими.
Первым антибиотиком, выделенным в 1943 г. из актиномицетов, был стрептомицин. Описание стрептомицина отнесено к разделу противотуберкулезных химиотерапевтических средств.
В 1947 г. из культуры лучистого грибка Actinomyces venezuelae был выделен антибиотик, получивший название хлорамфеннкола. По сравнению с пенициллином и стрептомицином (см. ниже) этот антибиотик отличался необычайно широким антибактериальным спектром, что сразу вызвала к нему очень большой интерес. К хлорамфениколу оказались чувствительны возбудители очень многих заболеваний: стафилококки, пневмококки, стрептококки, гонококки, возбудители брюшного и сыпного тифа, бруцеллеза, дизентерии, коклюша, трахомы, клещевого возвратного тифа, сифилиса и др.
Химическое строение хлорамфеникола было расшифровано в 1949 г. Следует подчеркнуть тот факт, что хлорамфеникол был первым природным соединением, в котором обнаружены нитрогруппа и неионогенный хлор.
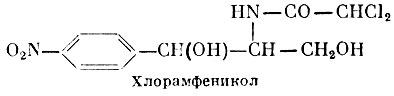
Хлорамфеникол
В Советском Союзе выпускается два препарата: синтомицин и левомицетин. Левомицетин полностью идентичен естественному антибиотику хлорамфениколу. Синтомицин представляет собой рацемическую смесь правого и левого изомеров хлорамфеникола. Химпотерапевтической активностью, проявляющейся преимущественно в виде бактериостатического эффекта, обладает только левый изомер, правый изомер в отношении микробов неактивен. Установлены качественные различия в действии изомеров на центральную нервную систему. Правый изомер оказывает на центральную нервную систему главным образом возбуждающее действие, левый — преимущественно угнетающее. Местно левомицетин не оказывает раздражающего действия на ткани. При введении внутрь левомицетин хорошо всасывается. Через 30 минут после приема он уже обнаруживается в крови, достигая максимума через 2—4 часа. Терапевтическая концентрация в крови удерживается 6—8 часов, что позволяет назначать препараты с лечебной целью внутрь через каждые 6—8 часов. Содержание левомицетина в крови можно определять микробиологическим или химическим путем на основании определения концентрации нитросоединений в крови. И тем и другим методом определяются совпадающие результаты. Выделяется из организма левомицетин преимущественно почками. После однократного введения выделение происходит в течение суток.
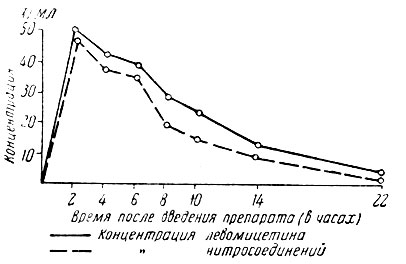
Рис.73. Концентрация левомицетина и нитросоздиненяй в сыворотке крови человека после однократного введения 3 г антибиотика
Токсичность хлорамфеникола в общем невелика. При внутривенном введении она значительно выше, чем при других способах применения. Так, внутривенная инъекция собакам 150 мг/кг левомицетина вызывает гибель животных при явлениях падения кровяного давления и остановки дыхания.
Показания к применению левомицетина и синтомицина одинаковы. В соответствии с антибактериальным спектром они применяются при многих инфекционных заболеваниях, а также в хирургической практике энтерально и местно при раневых инфекциях и других гнойных процессах (карбункулы, фурункулы, остеомиелиты). При необходимости лечение антибиотиками сочетается с хирургическими методами лечения (вскрытие флегмон, гнойников). Синтомицин и левомицетин оказывают в равной степени высокий химиотерапевтический эффект, но в связи с тем что в составе синтомицина имеется правый изомер, не обладающий активностью в отношении микробов, он назначается в несколько больших дозах по сравнению с левомицетином. Лечение проводится курсами.
У большинства микробов, чувствительных к левомицетину, в процессе лечения образуется лекарственная устойчивость (резистентность) к антибиотику, но привыкание микробов развивается значительно медленнее, чем к стрептомицину.
При приеме синтомицина и левомицетина могут иметь место побочные явления. Они выражаются в образовании метгемоглобина, уменьшении числа эритроцитов, снижении процента гемоглобина, сонливости, депрессии, сыпях, в развитии кандидозов.
Препараты
Левомицетин (Laevomycetinum) (Б). Бесцветные кристаллы горького вкуса, трудно растворимые в воде. Назначается внутрь по 0,25—0,75 г до 5 раз в сутки. Длительность лечения составляет 4—10 дней, при некоторых заболеваниях, когда возможны рецидивы, препарат применяют в течение 2—3 недель. Для лечения трахомы местно применяется 1% эмульсия.
Высшие дозы: 1 г (4 г).
Синтомицин (Synthomycinum) (Б). Белый кристаллический порошок горького вкуса, плохо растворимый в воде. Назначается внутрь по 0,5—1 г на прием до 6 раз в сутки. В глазной практике при трахоме и в хирургии при различных гнойничковых поражениях кожи применяется в эмульсии, содержащей 1—10% синтомицина.
Высшие дозы: 1,5 г (6 г).
Эусинтомицин (Eusynthomycinum) (Б). Стеариновый эфир синтомицина, кристаллический порошок, нерастворимый в воде. В отличие от синтомицина не обладает горьким вкусом. В кишечнике расщепляется с образованием синтомицина и стеариновой кислоты. При приеме эусинто-мицина в крови определяется более низкая концентрация препарата, чем при введении самого синтомицина. В связи с этим эусинтомицин назначается в дозах, несколько превышающих дозы синтомицина. Препарат удобен для применения в детской практике.
Тетрациклиновые антибиотики
К антибиотикам тетрациклинового ряда относятся тетрациклин, террамицин и биомицин (ауреомицин), очень близкие между собой по химическому строению и действию на микробы.
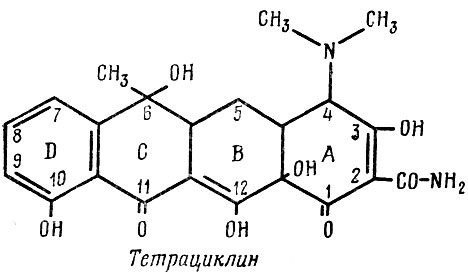
Тетрациклин
Ауреомицин (или хлортетрациклин) отличается от тетрациклина наличием в молекуле одного атома неионного хлора (в положении 7). Террамицин (или окситетрациклин) по сравнению с тетрациклином содержит в молекуле одну дополнительную гидроксильную группу (в положении 5).
Ауреомицин продуцируется лучистым грибком Actynomyces aureofaciens. Он был выделен в 1948 г. Желтая окраска мицелия грибка, образующего антибиотик, а также самого кристаллического антибиотика послужила причиной того, что антибиотик был назван ауреомицином, что означает «желтое вещество из грибка». В Советском Союзе был создан препарат, по строению и действию сходный с ауреомицином и получивший название биомицина.
Биомицин обладает широким антибактериальным спектром. Оказывая бактериостатическое действие, он подавляет рост многих грамположительных и грамотрицательных бактерий в разведении 1 : 100 000, 1 : 1 000 000 и выше. Бактерицидного действия на микробы биомицин не оказывает. Антибактериальный спектр биомицина очень сходен с таковым левомицетина. Различие состоит в том, что левомицетин оказывается более эффективным при заболеваниях, вызванных грамотрицательными бактериями, а биомицин дает более выраженный терапевтический эффект при заболеваниях, обусловленных грамположительными бактериями.
При изучении этих антибиотиков было установлено, что они проявляют неодинаковую активность в отношении микробов при проведении пробирочных опытов на культурах бактерий и в условиях целого организма. Биомицин в пробирке подавляет рост туберкулезной бактерии в равной степени со стрептомицином, в то время как в организме он не оказывает влияния на течение туберкулезной инфекции. Биомицин в организме действует на стафилококка в 5 раз сильнее, чем в пробирке. Левомицетив оказался более эффективным, чем биомицин, при лечении брюшного тифа, хотя опыты в пробирках показывали равный эффект. Эти факты подчеркивают значение реакции организма в терапевтическом эффекте антибиотиков. Привыкание большинства патогенных бактерий к биомицину наступает позднее, чем к стрептомицину.
Биомицин быстро всасывается из желудочно-кишечного тракта. В течение 6—7 часов в крови удерживается терапевтическая концентрация. Биомицин проникает в спинномозговую жидкость.
Препарат эффективен при самых разнообразных инфекционных заболеваниях. Он успешно применяется при заболеваниях, вызванных пенициллино и стрептомициноустойчивыми формами микробов. При сыпном тифе наблюдается постепенное (литическое) падение температуры, череа 2 суток исчезают основные симптомы. Биомицин эффективен при бруцеллезе, амебной дизентерии, применяется также при бациллярной дизентерии, тяжелых формах пневмонии, бронхитах, при септических состояниях. В хирургической практике биомицин используют местно при лечении инфицированных ран, флегмон, абсцессов и других гнойных заболеваний.
Биологическая активность биомицина определяется в единицах действия (ЕД). За 1 единицу действия принимается биологическая активность 1 мг химически чистого биомицина основания. Активность 1 мг солянокислого биомицина соответствует 930 ЕД.
Биомицин назначается внутрь. Лечение проводят курсами различной длительности. Внутривенно назначать его опасно из-за возникающих тромбофлебитов; токсичность препарата в этом случае возрастает в 5 раз. Все же иногда для спасения больного возникает необходимость внутривенного введения биомицина. В этих случаях используется специальный растворимый препарат антибиотика, выпускаемый в стерильных флаконах. При приеме биомицина нередко наблюдаются побочные явления: понижение аппетита, тошнота, рвота, жидкий стул, кожные сыпи, кандидозы.
Террамицин является продуктом жизнедеятельности Actinomyces rimosus. Антибактериальный спектр его очень близок к спектру биомицина. При приеме внутрь террамицин быстро всасывается. Максимальная концентрация его в крови определяется уже через час после введения. Терапевтическая концентрация в крови удерживается не менее 5 часов. Высокое содержание террамицина установлено в желчи. Значительна» часть введенного внутрь препарата выводится кишечником и почками,
Показания к применению, а также побочные явления те же, что и при назначении биомицина. 1 мг террамицина соответствует 1000 ЕД. Назначают препарат внутрь, лечение проводится курсами. Террамицин применяется также в глазной практике в виде мазей.
Тетрациклин получается путем ферментации или синтетически. По антибактериальному спектру он стоит близко к биомицину и террамицину, горьким вкусом не обладает, длительнее, чем другие антибиотики этой группы, определяется в терапевтической концентрации в крови, хорошо всасывается из желудочно-кишечного тракта; назначается внутрь и местно в виде растворов и мазей.
По сравнению с пенициллином и стрептомицином все антибиотики этой группы длительнее циркулируют в крови. По некоторым экспериментальным данным, внутренние органы, особенно печень, депонируют тетрациклины, в меньшей степени имеет место связывание антибиотиков белками сыворотки. Комплекс белок+тетрациклин легко диссоциирует. Снижение концентрации антибиотика в крови способствует его поступлению из внутренних органов в кровь.
Препараты
Биомицин хлористоводородный (Biomycinum hydrochloricum). Кристаллический порошок золотисто-желтого'цвета. Растворимость в воде примерно 1 : 100. Назначается по 0,1—0,2 г (100 000—200 000 ЕД) 4—6 раз в сутки за полчаса до еды. Для наружного применения готовят растворы (0,1—0,5%) и мазь (0.1—0,5%).
Высшая суточная доза: 2 г (2 000 000 ЕД).
Террамицин (Terramycimim). Хлоргидрат окситетрациклина — кристаллический порошок, растворимый в воде. Назначается внутрь по 0,1—0,5 г 3—4 раза в день. Мазь готовят с содержанием 5000 или 10 000 ЕД в 1 г.
Высшая суточная доза: 2 г.
Тетрациклин (Tetracyclinum). Основание тетрациклина назначается внутрь по 0,1—0,15 г 4—б раз в сутки (в таблетках, капсулах). Хлор-гидрат тетрациклина используется для приготовления глазных капель (0,5%) и мазей (1—2%).
Высшая суточная доза: 2 г.
Другие антибиотики
Альбомицин представляет собой продукт жизнедеятельности Streptomyces subtropicus. Впервые получен в Советском Союзе путем выделения из культуральной жидкости, на которой выращивается грибок.
Альбомицин обладает широким антибактериальным спектром, подавляя как грамположительные, так и грамотрицательные бактерии. Среди них стафилококки, гемолитические стрептококки, пневмококки, дизентерийные бактерии, пневмобактерии Фридлендера и ряд других. Туберкулезные бактерии и риккетсии к альбомицину устойчивы. Альбомицив активен в отношении пенициллиноустойчивых форм микробов (стафилококков, пневмококков и некоторых других), что свидетельствует о различии механизма действия на бактерии пенициллина и альбомицина. В связи с этим альбомицин показан для лечения септических заболеваний, возбудителем которых являются устойчивые к пенициллину формы микробов.
Отличительной особенностью альбомицина является его малая токсичность. Животные переносят большие дозы альбомицина при внутривенном введении, и при этом не наблюдается каких-либо признаков токсического действия. Смертельные дозы для альбомицина в условиях эксперимента не установлены. Длительное введение препарата в организм не оказывает отрицательного влияния на органы и ткани. Альбомицин, помимо влияния на микробы, стимулирует защитные силы организма, в частности усиливает фагоцитоз.
Основное количество введенного альбомицина выделяется из организма в течение 6—7 часов почками, меньшая часть связывается белками крови и выделяется из организма постепенно, в течение 2—3 суток.
Активность альбомицина определяют микробиологическим методом и выражают в единицах действия (ЕД). За единицу действия принимают активность такого количества альбомицина, которое подавляет рост стафилококка стандартного штамма в 1 мл питательного агара. По активности 1 мг альбомицина соответствует 300 000 ЕД. Препарат вводят подкожно 2 раза в сутки. Длительность лечения 7—20 дней. При хирургических заболеваниях (перитонит) альбомицин вводят иногда через дренаж непосредственно в брюшную полость.
Отмечается хорошая переносимость препарата больными. Аллергические реакции возникают редко и выражаются сыпями типа крапивницы. Побочные явления устраняются назначением противогистаминных препаратов. Альбомицин можно сочетать с другими антибиотиками, а также с сульфаниламидами. Антибиотик чаще применяется в детской практике.
Новый антибиотик эритромицин перспективен, поскольку он оказался аффективным при лечении инфекций, вызванных устойчивыми к пенициллину микробами, а также при энтероколитах, возникающих как побочное явление в процессе лечения тетрациклиновыми антибиотиками. Следует учитывать, что заболевания, вызванные устойчивым к пенициллину стафилококком, протекают чрезвычайно тяжело с высоким процентом смертности.
Препарат назначают внутрь каждые б часов. К эритромицину довольно быстро развивается устойчивость микробов.
Некоторые антибиотики, как грамицидин, колимицин, обладают широким - антибактериальным спектром, но из-за токсического действия не могут быть использованы для химиотерапии общих инфекций. Грамицидин вызывает гемолиз и флебиты. Введение внутримышечно колимицина сопровождается поражением VIII пары черепных нервов. Эти антибиотики применяются местно и более подробно рассмотрены в разделе «Антисептические средства».
Препараты
Альбомицин (Albomycinum). Порошок желтого или коричневого цвета, хорошо растворим в воде. Детям вводят подкожно по 10О 000 — 200 000 ЕД на 1 кг веса в сутки в 2 приема. Растворы готовят непосредственно перед употреблением из расчета 500 000 ЕД в 1 мл. В качестве растворителя применяют дважды дистиллированную стерильную воду. Взрослым вводят до 10 000 000 ЕД в сутки.
Выпускают в ампулах с различным количеством альбомицина.
* * *
В борьбе с инфекциями антибиотики сыграли большую роль. В нашей стране благодаря применению этих препаратов снизилась и продолжает непрерывно снижаться инфекционная заболеваемость. Но, используя антибиотики в качестве лечебных средств, необходимо также всеми мерами повышать защитные свойства организма. Сами антибиотики должны применяться строго по показаниям с учетом индивидуальных свойств каждого антибиотика с точки зрения его антибактериального спектра и вызываемых им побочных реакций. Особого внимания и осведомленности требует комбинированное применение антибиотиков, при котором в отношении возбудителя могут наблюдаться явления как синергизма, так и антагонизма. Антибиотики следует применять только по назначению врача и отпускать из аптек исключительно по рецептам. Неумелое использование антибиотиков приводит к развитию лекарственной устойчивости микробов, и тем самым высокая эффективность препарата утрачивается. Особенный вред приносит назначение антибиотиков при легких заболеваниях, которые купируются другими средствами, а часто проходят и без лечения. Лечение антибиотиками в этих случаях обычно проводят неполной курсовой дозой, способствующей лишь ускорению образования резистентных форм. В то же время при повторном применении антибиотиков побочные реакции и явления непереносимости возникают значительно чаще.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'