
Заключение
Все изложенное в данной книге говорит об определенных успехах науки в раскрытии молекулярных механизмов действия многих ядовитых веществ и выяснении сущности процессов их превращения в организме. Это в свою очередь обусловило реальные возможности создания эффективных противоядий, которые или уже стали практически используемыми препаратами, или еще находятся в стадии экспериментальной разработки. При описании действия противоядий мы не разграничивали их по такому признаку и не акцентировали внимание на лечебной стороне вопроса, поскольку стремились ознакомить читателя прежде всего с важнейшими механизмами антидотного эффекта в том виде, в каком они представляются в настоящее время. И здесь необходимо особо подчеркнуть, что успешное специфическое воздействие на токсический процесс с помощью антидотов является хотя и весьма надежным, но лишь одним из нескольких реально значимых принципов борьбы с отравлениями. Это тем более важно иметь в виду, что в настоящее время еще не существует противоядий при интоксикациях многими распространенными ядами: дихлорэтаном, бензолом и рядом его производных, высокотоксичными веществами растительного и животного происхождения и др. Современную практическую токсикологию невозможно представить без многих других неотложных мероприятий (назовем их неспецифическими) по предупреждению и лечению интоксикаций. Не касаясь конкретных показаний к проведению этих мероприятий, перечислим важнейшие из них.
- Экстренное прекращение дальнейшего поступления (всасывания) яда во внутренние среды организма (промывание желудка, вызывание рвоты, удаление яда из кишечника, а также его нейтрализация при попадании в глаза, на кожу и слизистые оболочки).
- Ускоренное выведение из организма уже всосавшегося яда и его токсичных метаболитов для максимального уменьшения их количества в крови и тканях. С этой целью при тяжело протекающих острых отравлениях применяются:
- а) форсированный диурез, т. е. резкое усиление выделительной функции почек как естественного способа очищения организма от токсичных веществ, что достигается введением отравленному больших количеств жидкости и растворов осмотически активных веществ, а также диуретических средств; при ряде тяжелых отравлений форсированный диурез проводится совместно с алкалинизацией (ощелачиванием) плазмы и мочи, что препятствует задержке ядов в тканях, повышает растворимость и тормозит их обратное всасывание в почках;
- б) увеличение продукции желчи клетками печени и усиление работы органов дыхания с помощью соответствующих лекарственных средств;
- в) гемодиализ (избирательный обмен различных веществ между плазмой крови и специальным раствором электролитов через поры полупроницаемой мембраны), перитонеальный диализ (введение в брюшную полость гипертонического раствора электролитов, в который ядовитые вещества переходят из крови через брюшину, выполняющую функцию диализирующей мембраны);
- г) гемосорбция и ее разновидности - плазмо и лимфосорбция (очищение крови от чужеродных и балластных эндогенных веществ посредством подключения кровеносного русла к специальному аппарату с сорбирующими веществами, что одновременно обеспечивает поддержание детоксикационной функции печени); по быстроте и эффективности гемосорбция теперь ставится на первое место из всех способов выведения токсичных веществ из организма.
- Восстановление и обеспечение нормального функционирования жизненно важных систем и органов: кровообращения, дыхания, центральной нервной системы, печени, почек, а также гуморальной среды организма (электролитный баланс, кислотно-щелочное равновесие, водный обмен).
- Введение кислорода в организм отравленного как метод патогенетического лечения гипоксических состояний, практически возникающих при всех острых интоксикациях. Необходимым условием успешного кислородного лечения является устранение (или по крайней мере уменьшение) токсических нарушений транспорта кислорода в организме.
Опыт показывает, что экспериментальные и клинические данные о разнообразных типах специфического воздействия на токсический процесс могут считаться достоверными лишь тогда, когда позволяют на молекулярном уровне оценить характер взаимодействия ядов, - реактивных структур организма и антидотов. Иными словами, особую токсикологическую значимость приобретает анализ сущности химических (биохимических) и физико-химических процессов, протекающих при таком взаимодействии. Сейчас есть достаточно оснований полагать (и в этом мог убедиться читатель), что наибольшую практическую ценность и перспективность имеют те антидоты, которые в "точках приложения" ядов действуют выборочно на определенные биологические структуры и позволяют тем самым вмешиваться в интимные механизмы жизнедеятельности, в частности в функцию передатчиков нервного возбуждения и рецепторных образований организма. Несомненно также большое значение противоядий, активно влияющих на течение различных обменных процессов.
В числе всех этих так называемых функциональных противоядий мы рассмотрели вещества, препятствующие действию яда на рецепторные структуры или блокирующие это действие (атропиноподобные соединения, адреноблокаторы, обратимые ингибиторы ферментов); реактивирующие биоструктуры с последующей окончательной или временной детоксикацией яда (оксимы, унитиол, цистамин); конкурирующие с ядом за связь с рецепторами (кислород, структурные аналоги токсичных лекарств); замещающие биоструктуры, поврежденные или утраченные под воздействием яда (пиридоксин, цитохром С, хлорид кальция); активаторы и ингибиторы ферментов, метаболизирующих яды (препарат SKF-525A, антиоксиданты), и ряд других. Некоторые из них являются анти-дотами многостороннего действия и, значит, могут использоваться при различных отравлениях или яда воздействовать на один и тот же токсический процесс разными путями. Например, глюкоза и метиленовый синий - антицианиды и в то же время восстановители метгемоглобина. Кроме того, глюкоза может быть заместительным антидотом при инсулиновой интоксикации, а метиленовый сивый влиять на процессы тканевого окисления, нарушенные ядами. Здесь уместно отметить, что в последнее время все большее значение в качестве противоядий многостороннего действия приобретают антиоксиданты. В частности, такие вещества, как токоферол, селенит натрия, цистамин и другие содержащие серу аминокислоты, снижают токсичность отдельных ФОС, воздействуя, по-видимому, на соответствующие ферменты, подобно препарату SKF-525A. Кроме того, они тормозят окислительные превращения некоторых токсичных химических соединений в вещества, избирательно влияющие на биоструктуры. Например, антиоксиданты препятствуют окислению анилина в метгемоглобинообразующий метаболит. Однако наличие разнообразных антидотов непрямого типа действия не снижает практической роли препаратов, обезвреживающих яды в организме химическим (физико-химическим) путем. Именно эти противоядия по традиции принято использовать в первую очередь прежде всего из-за доступности способов применения и достаточно уверенного прогнозирования их действия.
Подводя итог рассмотрению антидотных средств, приходится констатировать некоторое отставание практики лечения отравлений от достижений экспериментальной токсикологии. На это, например, обратил внимание академик АМН СССР С. Н. Голиков,* который, в частности, указал на неиспользуемые реальные возможности применения многих новых холинолитиков и их комбинаций, значительно превосходящих по своей активности атропин и в то же время лучше переносимых человеком. К сожалению, даже в некоторых токсикологических практических руководствах и учебных пособиях подчас не описываются отдельные известные и хорошо зарекомендовавшие себя на практике антидоты (например, актарсин как антидот мышьяковистого водорода, а также цистамин и метиленовый синий как активные средства восстановления метгемоглобина).
*( Голиков С. Н. Профилактика и терапия отравлений фосфорорганическими инсектицидами. М.: Медицина, 1933)
Не вызывает сомнения, что точная диагностика и наличие быстро и надежно действующего антидота являются необходимыми условиями эффективной борьбы с отравлениями. Но специфическое вмешательство в течение отравления дает желаемый результат тогда, когда антидот вводится в нужном количестве и в наиболее подходящие сроки. В этой связи интересно рассмотреть в динамике воздействие яда и антидота на организм. Можно представить острый токсический процесс графически в виде кривой, которая отображает направление сдвига физиологической функции (например, кровообращения, дыхания, нервно-мышечного аппарата) от нормального ее уровня до максимального проявления с последующим спадом (рис. 20). Если антидот введен в начальном периоде развития отравления, то, будучи антагонистом яда, он способствует замедлению или остановке токсического процесса. Здесь имеет значение доза антидота: когда она недостаточна, то действие яда продолжается, а когда слишком велика то может снизить уровень физиологических функций ниже нормального. На высоте развития интоксикации лечебный эффект может быть достигнут с помощью большей дозы антидота, который действует медленнее. При этом вероятность возврата к исходному уровню уже уменьшается. Если же противоядие начинают применять на последней стадии отравления, когда уже сказывается истощение энергетических ресурсов эффекторных органов и их избыточная функция проявляется в меньшей степени, то взаимоотношения яда и антидота принципиально меняются: из антагонистов они превращаются в синергистов. Здесь еще большее значение приобретает выбор дозы антидота, так как при его передозировке может быть ускорено наступление рокового исхода. Конечно, на этой стадии эффективность антидотного лечения резко снижается. Такое представление о динамической взаимосвязи яда и антидота оказывается справедливым в отношении многих остро протекающих интоксикаций. Из него следует что одной из труднейших задач которую призвана решить токсикология, - является разработка в каждом конкретном случае временных и количественных рекомендаций по использованию антидотов.
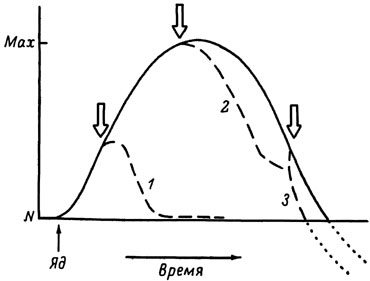
рис. 20. Схема воздействия яда и антидота на физиологическую систему во времени при остро протекающем отравлении. N - нормальный уровень функционирования физиологической системы; Мах - максимальный уровень функционирования физиологической системы; сплошная линия - направление сдвига физиологической функции; пунктирные линии - спад физиологической функции ниже нормы; полые стрелки - время введения антидота; прерывистые линии - замедление токсического процесса и нормализация физиологической функции после введения антидота в начальный период действия яда (1) и на высоте интоксикации (2), ускорение спада физиологической функции после введения антидота на последнем этапе действия яда (3)
До настоящего времени распространенным еще методом изыскания антидотов, как и других лекарственных веществ, является эмпирический их поиск среди многочисленных продуктов химического синтеза и природных соединений, когда отбираются те из них, которые обладают нужными фармакологическими свойствами. Данный метод получил в литературе название скрининга, что в переводе с английского означает "просеивание через решето". Большое значение в этой связи имеет установление выраженности антидотного эффекта у различных веществ в зависимости от их химического строения, важнейших физико-химических параметров, характера превращений в организме.* Такое направление экспериментальной токсикологии показывает, что не следует отказываться от поисков антидотов в тех случаях, когда еще не известны основные биохимические проявления токсических процессов. Известны примеры, когда новые фармакологические эффекты у лекарственных веществ выявляются подчас неожиданно, уже при их клиническом применении. Эти случайные открытия нередко могут определить пути синтеза ранее неизвестных биологически активных веществ, в том числе противоядий. Так, обнаружение возбуждения и эйфории у больных, получавших ипрониазид как противотуберкулезное средство, привело к открытию новой группы психотропных препаратов - антидепрессантов - Ингибиторов моноаминоксидазы. Еще один пример такого рода - установление специфического действия антабуса при алкогольной интоксикации: повышение чувствительности к алкоголю под влиянием этого препарата было впервые обнаружено при его испытании в качестве антигельминтного (противоглистного) средства.** Однако опыт показывает, что только раскрытие молекулярных механизмов действия ядов может считаться реальной предпосылкой целенаправленного создания антидотов. И здесь главное значение приобретает такой синтез биологически активных веществ, который основан на планировании определенных их свойств. Именно этот принцип гарантирует получение веществ с заранее известной или предполагаемой фармакологической активностью.
*( Мизюкова И. Г., Петрунъкин В. Е. О подходах к изысканию средств антидотной терапии отравлений химической этиологии. - В кн.: Общие вопросы промышленной токсикологии. М., 1967, с. 153-157)
**( Машковский М. Д. Современные принципы поисков лекарственных веществ. - ЖВХО, 1970, № 2, с. 132-143)
Анализируя сущность направленного синтезирования лекарств, академик АМН СССР М. Д. Машковенский рассматривает следующие основные его разновидности:
- 1) воспроизведение биогенных физиологически активных веществ (ферментов, витаминов, гормонов, аминокислот, биогенных аминов) и синтез соединений, влияющих на их активность;
- 2) химическая модификация молекул известных физиологически активных соединений, в тем числе противоядий, с целью придания им новых свойств;
- 3) изыскание лекарств среди физиологически активных продуктов их превращения в организме.
Что касается лекарственных средств специфического воздействия на течение и исход отравлений, то практическое значение могут иметь по крайней мере следующие основные пути их создания.* Первый путь - создание химических веществ, обладающих способностью определенным образом реагировать с теми или иными биосубстратами, появляющимися в организме при развитии патологического (токсического) процесса, и тем самым вызывать полезные биохимические сдвиги. Этот путь можно проиллюстрировать механизмом действия таких эффективных антидотов, как реактиваторы холинэстераз и метгемоглобинообразующие вещества. Второй путь основан на метаболическом принципе - создание веществ, способных биохимически регулировать (снижать или увеличивать) скорость синтеза какого-либо биосубстрата, если при отравлении этот процесс нарушен. Это прежде всего активаторы и ингибиторы ферментов, - определяющих течение процессов превращений ядов в организме. Третий путь основан на заместительном принципе: если в результате токсического процесса происходит уменьшение содержания в организме какого-либо биосубстрата, то последний может быть введен извне, как это было видно на примерах антидотного действия ферментных препаратов и некоторых биоэлементов.
*( Павлов В.А. Биохимические принципы взыскания Лекарственных веществ. - ЖВХО, 1973, № 2, с. 122-124)
Несомненно, что работы по созданию средств целенаправленного воздействия на различные интоксикации не могут оставаться в стороне от последних достижений медико-биологических наук. Так, недавно в нашей страна в клинических условиях были впервые в мире успешно испытаны иммобилизованные ферменты-биокатализаторы, соединенные с веществами-носителями, безвредными для организма. Тем самым удалось резко увеличить сроки биохимической активности ряда ферментов и долгое время поддерживать их концентрацию на заданном уровне в определенном органе или ткани. Как подчеркнул академик Е. И. Чазов,* это свидетельствует о том, что мы, очевидно, находимся на пороге новых подходов к дозировке и применению многих препаратов, изменения стратегии лекарственной терапии. Можно полагать, что использование метода иммобилизованных ферментов поможет решить ряд задач диагностики и специфического лечения отравлений. Немалые возможности для токсикологии появляются в связи с расширяющимся диапазоном применения липосом - закрытых однослойных или многослойных концентрических липидных частиц размером 30-100 нм, содержащих воду с растворенными в ней веществами. В настоящее время они рассматриваются как особая лекарственная форма для направленного транспорта фармакологических веществ в организме. Например, было показано, что применение липосом, - инкапсулированных раствором комплексонов, ускоряет выведение тяжелых металлов, удлиняет сроки действия антидотов и способствует их проникновению через клеточные мембраны.**
*( Чазов. Е. В содружестве с природой, - Правда, 3 мая 1979, с. 4
**( Тенцова А. И. Ковалева Н. С., Ярова Е. А., Ивков И. И. Липосомы, возможности их применения в фармации фармакологии. - Фармация, 1970, № 3, с. 82-85)
Большие перспективы в работе по созданию антидотных средств воздействия на токсический процесс дает новая область науки - иммунофармакология, которая, в частности, призвана решать проблему направленного образования в организме защитных белковых структур (антител) в ответ на введение физиологически активных соединений, в том числе ядов.* Известно, что абсолютное большинство лекарственных препаратов и ядов при парентеральном введении не являются антигенами, т. е. не индуцируют в организма продукцию антител. Нo если эти вещества присоединить к микроносителю, например белку, то их можно превратить в высокоантигенные, Тоща при последующем токсическом воздействии организм будет обладать специфическими защитными механизмами, т, е. возникнет возможность имунного ответа полезного вещества (антитело) на действие вредного вещества (яд). Следовательно, можно получить и практически использовать антитела к различным химическим соединениям, в том числе фармакологическим агентам. Так, в нашей стране в научно-исследовательском институте по биологическим испытаниям химических соединений профессором И. Е. Ковалевым и его сотрудниками получены и испытаны такого рода антитела к морфину, барбитуратам, некоторым эндогенным веществам. Помимо создания качественно новых типов антидотов, иммуно-фармакология разрабатывает оригинальные способы решения таких важных токсикологических и фармакологических задач, как например, изучение механизмов действия ядов, пролонгирование нахождения в крови того или иного полезного вещества, выявление сущности биотрансформации и токсикокинетики чужеродных веществ.
*( Ковалев И. Е., Пелевая О. Ю, Антитела к физиологически активным соединениям. М.: Медицина, 1981)
Таким образом, есть достаточно оснований предсказать создание в ближайшее время новых специфических средств и методов борьбы с отравлениями. Такая уверенность проистекает также из общей оценки токсикологии как быстро развивающейся науки. Залогом успеха в этом нелегком, но многообещающем и увлекательном деле является тесное взаимодействие токсикологии с близкими научными дисциплинами, прежде всего - фармакологией биохимией, фармацевтической химией.
|
ПОИСК:
|
© PHARMACOLOGYLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://pharmacologylib.ru/ 'Библиотека по фармакологии'